Ішек флорасы - Википедия - Gut flora

Ішек флорасы немесе ішек микробиотасы болып табылады микроорганизмдер оның ішінде бактериялар, архей және саңырауқұлақтар өмір сүреді ас қорыту жолдары адамдардың[1] және басқа жануарлар, соның ішінде жәндіктер. Асқазан-ішек метагеном барлығының жиынтығы геномдар ішектің микробиота.[2][3] Ішек - негізгі орналасуы адамның микробиотасы.[4]
Шолу
Адамдарда ішектің микробиотасы организмнің басқа аймақтарымен салыстырғанда ең көп бактериялар мен түрлердің көп мөлшеріне ие.[5] Адамдарда ішек флорасы туылғаннан кейін бір-екі жылдан кейін қалыптасады, осы уақытқа дейін ішек эпителийі және ішектің шырышты қабаты ол шығаратын заттар ішек флорасына төзімді, тіпті қолдау көрсететін және патогенді организмдерге кедергі болатын жолмен бірге дамыған.[6][7]
Кейбір ішектер арасындағы байланыс флора және адамдар тек қана емес комменсал (зиянсыз қатар өмір сүру), керісінше а мутуалистік қарым-қатынас.[4]:700 Кейбір адамның ішек микроорганизмдері иесіне пайда әкеледі ашыту диеталық талшық ішіне қысқа тізбекті май қышқылдары (SCFAs), мысалы сірке қышқылы және май қышқылы, содан кейін оларды иесі сіңіреді.[5][8] Ішек бактериялар синтездеуде де рөл атқарады В дәрумені және К дәрумені метаболиздену сияқты өт қышқылдары, стеролдар, және ксенобиотиктер.[4][8] SCFAs және олар шығаратын басқа қосылыстардың жүйелік маңызы ұқсас гормондар және ішек флорасы өзі сияқты жұмыс істейді эндокриндік орган,[8] және ішек флорасының реттелмеуі көптеген қабыну және аутоиммундық жағдайлармен байланысты болды.[5][9]
Адамның ішек микробиотасының құрамы уақыт өткен сайын, диета өзгерген кезде және жалпы денсаулық өзгерген сайын өзгереді.[5][9] A жүйелі шолу 2016 жылдан бастап пробиотикалық бактериялардың коммерциялық қол жетімді штамдарымен жүргізілген клиникаға дейінгі және кішігірім адам сынақтарын зерттеп, белгілі біреулерге пайдалы болуы мүмкін мүмкіндіктерді анықтады орталық жүйке жүйесінің бұзылуы.[10]
Жіктелімдері
Ішек микробиотасының микробтық құрамы ас қорыту жолында әр түрлі болады. Ішінде асқазан және жіңішке ішек, бактериялардың салыстырмалы түрде аз түрлері кездеседі.[11][12] The тоқ ішек, керісінше, Жердегі тіршілік ету ортасында тіркелген ең жоғары микробтық тығыздықты қамтиды[13] 10-ға дейін12 ішек мазмұнының бір граммына жасушалар.[11] Бұл бактериялар 300-ден 1000-ға дейін әртүрлі түрлері.[11][12] Алайда бактериялардың 99% -ы шамамен 30 немесе 40 түрден келеді.[14] Олардың ішекте көп болуының нәтижесінде бактериялар құрғақ массасының 60% құрайды нәжіс.[15] Саңырауқұлақтар, қарсыластар, архей, және вирустар ішек флорасында да бар, бірақ олардың қызметі туралы аз біледі.[16]
Ішектегі бактериялардың 99% -дан астамы анаэробтар, бірақ кекум, аэробты бактериялар жоғары тығыздыққа жету.[4] Бұл ішек флорасы шамамен жүз есе көп деп есептеледі гендер барлығы бар сияқты адам геномы.[17]
Ішектегі көптеген түрлер иелерінен тыс зерттелмеген, өйткені көпшілігі өсіруге болмайды.[12][14][18] Көптеген микробтардың негізгі түрлерінің саны аз болғанымен, микробтардың популяциясы әр түрлі адамдар арасында әр түрлі болуы мүмкін.[19] Жеке адамда микробтар популяциясы уақыт өте келе тұрақты болып қалады, дегенмен кейбір өзгерістер өмір салты, тамақтану режимі және жас өзгеруіне байланысты болуы мүмкін.[11][20] The Адамның микробиомасы жобасы сипаттамасын жақсылап сипаттауға кірісті микрофлора адамның ішегі және басқа дене орналасуы.
Төрт доминантты бактерия фила адамның ішегінде Firmicutes, Бактериоидтер, Актинобактериялар, және Протеобактериялар.[21] Бактериялардың көпшілігі тұқымдасқа жатады Бактероидтер, Клостридий, Фекалибактерия,[11][14] Эубактериялар, Руминококк, Пептококк, Пептострептококк, және Бифидобактериялар.[11][14] Сияқты басқа тұқымдастар Эшерихия және Лактобакиллус, аз мөлшерде бар.[11] Тұқымдас түрлер Бактероидтер тек ішектегі барлық бактериялардың шамамен 30% құрайды, демек, бұл тұқым иесінің жұмысында өте маңызды.[12]
Ішекте анықталған саңырауқұлақ тұқымдастарына жатады Candida, Сахаромицес, Аспергиллус, Пеницилл, Родоторула, Trametes, Плеоспора, Склеротиния, Буллера, және Галактомис, басқалардың арасында.[22][23] Родоторула жиі кездеседі ішектің қабыну ауруы уақыт Candida гепатит В циррозы және созылмалы В гепатиті бар адамдарда жиі кездеседі.[22]
Архей ашытудың бактериялық өнімдерінің метаболизмінде маңызды болатын ішек флорасының тағы бір үлкен класын құрайды.
Индустрияландыру микробиотаның өзгеруімен байланысты және әртүрліліктің төмендеуі кейбір түрлердің жойылуына әкелуі мүмкін; 2018 жылы зерттеушілер а биобанк адамның микробиотасы.[24]
Энтеротип
Ан энтеротип - тірі ағзалардың бактериологиялық негізінде жіктелуі экожүйе адамның ішек микробиомында жасына, жынысына, дене салмағына немесе ұлттық бөлінуіне байланысты емес.[25] Ұзақ мерзімді диета энтеротипке әсер ететін белгілер бар.[26] Адамның үш энтеротипі ұсынылды,[25][27] бірақ олардың құндылығына күмән келтірілді.[28]
Композиция
Бактериомалар
Асқазан
Асқазанның қышқылдығы жоғары болғандықтан, микроорганизмдердің көпшілігі онда тіршілік ете алмайды. Асқазанның негізгі бактериялық тұрғындары: Стрептококк, Стафилококк, Лактобакиллус, Пептострептококк.[4]:720 Хеликобактерия Бұл грамтеріс спиральды бактерия орнатады асқазанның шырышты қабаты созылмалы ауруды тудырады гастрит, және асқазан жарасының ауруы, және а канцероген үшін асқазан рагы.[4]:904
Ішек
| Әдетте адамның тоқ ішегінде кездесетін бактериялар[29] | |
| Бактериялар | Ауру (%) |
|---|---|
| Bacteroides fragilis | 100 |
| Bacteroides melaninogenicus | 100 |
| Bacteroides oralis | 100 |
| Enterococcus faecalis | 100 |
| Ішек таяқшасы | 100 |
| Энтеробактерия sp. | 40–80 |
| Клебсиелла sp. | 40–80 |
| Bifidobacterium bifidum | 30–70 |
| Алтын стафилококк | 30–50 |
| Лактобакиллус | 20–60 |
| Clostridium perfringens | 25–35 |
| Proteus mirabilis | 5–55 |
| Тетани Clostridium | 1–35 |
| Clostridium septicum | 5–25 |
| Pseudomonas aeruginosa | 3–11 |
| Salmonella enterica | 3–7 |
| Faecalibacterium prausnitzii | ? жалпы |
| Пептострептококк sp. | ? жалпы |
| Пептококк sp. | ? жалпы |
Аш ішекте асқазанның жақындығы мен әсер етуіне байланысты микроағзалардың мөлшері аз болады. Грам позитивті кокки және таяқша тәрізді бактериялар ащы ішекте кездесетін басым микроорганизмдер.[4] Алайда, ащы ішектің дистальды бөлігінде сілтілі жағдайлар бактериялардың грамтеріс бактерияларын қолдайды Энтеробактериялар.[4] Жіңішке ішектің бактериалды флорасы ішектің көптеген қызметтерін атқаруға көмектеседі. Бактерия флорасы ішектің дамуы мен пайдалылығына мүмкіндік беретін реттеуші сигналдар береді. Жіңішке ішекте бактериялардың көбеюі ішектің бұзылуына әкелуі мүмкін.[30] Сонымен қатар тоқ ішекте адам ағзасындағы ең үлкен бактериялық экожүйе бар.[4] Тоқ ішек пен нәжіс флорасының шамамен 99% -ы облигатты анаэробтардан тұрады Бактероидтер және Бифидобактериялар.[31] Тоқ ішектің микроорганизм популяциясын бұзатын факторларға антибиотиктер, стресс және паразиттер жатады.[4]
Флораның көп бөлігін бактериялар құрайды тоқ ішек[32] құрғақ массасының 60% құрайды нәжіс.[11] Бұл факт нәжісті үлгілерден нуклеин қышқылын бөліп алу арқылы кез-келген сынақтар мен эксперименттер үшін ішек флорасының идеалды көзі етеді және бактериялардың 16S rRNA гендік тізбегі бактериялардан тұрады. Тестілеудің бұл түрі көбінесе биопсия сияқты инвазивті техникадан гөрі қолайлы. 300 арасында[11] және 1000 әртүрлі түрлері ішекте өмір сүру,[12] шамамен 500-ге жуық бағамен.[33][34] Алайда, бактериялардың 99% -ы шамамен 30 немесе 40 түрден болуы ықтимал Faecalibacterium prausnitzii сау ересектерде ең көп кездесетін түрлер.[14][35]
Зерттеулер ішектің өзара байланысын көрсетеді флора және адамдар тек қана емес комменсал (зиянсыз қатар өмір сүру), бірақ керісінше а мутуалистік, симбиотикалық қарым-қатынас.[12] Адамдар ішек флорасы болмаса да өмір сүре алады,[33] сияқты микроорганизмдер көптеген пайдалы функцияларды орындайды ашыту пайдаланылатын энергия субстраты иммундық жүйе сияқты метаболизмнің соңғы өнімдері арқылы пропионат және ацетат, зиянды түрлердің көбеюіне жол бермеу, ішектің дамуын реттеу, иесіне дәрумендер шығару (мысалы биотин және К дәрумені ), және иелерді майларды сақтауға бағыттайтын гормондар шығарады.[4] Ішектің микробиотасының және оның микробиомасының немесе гендер жиынтығының кеңейтілген модификациясы мен теңгерімсіздігі семіздікпен байланысты.[36] Алайда, белгілі бір жағдайларда кейбір түрлер тудыруы мүмкін деп есептеледі ауру тудыруы арқылы инфекция немесе ұлғайту қатерлі ісік хост үшін тәуекел.[11][32]
Микобиома
Саңырауқұлақтар және қарсыластар сонымен қатар ішек флорасының бір бөлігін құрайды, бірақ олардың қызметі туралы аз белгілі.[37]
Виром
The адамның виромы негізінен бактериофагтар.[38]
Вариация
Жасы
Тіршілік барысында микробиомдық құрам эволюциясының жалпы заңдылықтары бар екендігі дәлелденді.[39] Жалпы алғанда, нәжіс үлгілерінің микробиоталық құрамының әртүрлілігі балаларға қарағанда ересектерде едәуір жоғары, дегенмен балалар арасындағы айырмашылық балаларда ересектерге қарағанда жоғары.[40] Микробиотаның ересек тәрізді конфигурацияға дейін жетілуінің көп бөлігі өмірдің алғашқы үш жылында жүреді.[40]
Микробиомның құрамы өзгерген сайын, ішекте пайда болатын бактериялық белоктардың құрамы да өзгереді. Ересек микробиомаларда ферменттеуге, метаногенезге және аргинин, глутамат, аспартат және лизин метаболизміне қатысатын ферменттердің жоғары таралуы анықталды. Керісінше, нәресте микробиомаларында доминантты ферменттер цистеин метаболизміне және ашыту жолдарына қатысады.[40]
Диета
Зерттеулер мен статистикалық талдаулар ішек микробиотасындағы бактериялардың әр түрлі тұқымдарын және олардың қоректік заттармен байланысын анықтады. Ішек микрофлорасы негізінен үшеуінен тұрады энтеротиптер: Превотелла, Бактероидтер, және Руминококк. Әрбір микробтық қауымдастық концентрациясы мен диета арасында байланыс бар. Мысалға, Превотелла көмірсулармен және қарапайым қанттармен байланысты Бактероидтер ақуыздармен, амин қышқылдарымен және қаныққан майлармен байланысты. Муцинді ыдырататын арнайы микробтар иесінің көмірсуларымен бірге тіршілік етеді.[41] Диетаға байланысты бір энтеротип басым болады. Диетаны өзгерту түр санының сәйкесінше өзгеруіне әкеледі.[26]
Вегетариандық және вегетариандық диеталар
Өсімдік тектес диеталар әр түрлі болғанымен, вегетариандық және вегетариандық диеталар үлгілері ең кең таралған. Вегетариандық диеталар ет өнімдерін қоспағанда, жұмыртқа мен сүт өнімдерін алуға мүмкіндік береді, ал вегетариандық диеталар жануарлардан алынатын өнімдердің барлық түрлерін жоққа шығарады. Вегетариандық және вегетариандық диеталар ет жегіштерден ерекшеленетін микробиом жасайды, бірақ екеуінің арасында айтарлықтай айырмашылық жоқ.[42][сенімсіз медициналық ақпарат көзі ме? ] Ет пен жануарлардан алынатын өнімдердің айналасында орналасқан диеталарда олардың көп мөлшері бар Алистиптер, Билофила және Бактероидтер олар өтке төзімді және ішектің қабынуына ықпал етуі мүмкін. Диетаның бұл түрінде топ Firmicutes, бұл диеталық өсімдік полисахаридтерінің метаболизмімен байланысты, төмен концентрацияда кездеседі.[43] Керісінше, өсімдік тектес материалдарға бай диеталар ішек микробиомының әртүрлілігімен байланысты және олардың көптігі Превотелла, өтке төзімді түрлерден гөрі, талшықтарды ұзақ уақыт өңдеуге жауапты.[44][сенімсіз медициналық ақпарат көзі ме? ] Диетаны ішек микробиомының құрамын салыстырмалы түрде қысқа уақыт кезеңінде өзгерту үшін қолдануға болады. Алайда, егер ауру немесе аурумен күресу үшін микробиомды өзгерткісі келсе, диетадағы ұзақ мерзімді өзгерістер ең сәтті болып шықты.[43]
География
Ішек микробиомының құрамы популяциялардың географиялық шығу тегіне байланысты. Келісімнің өзгерістері Превотелла, өкілдігі уреаза ген және глутамат синтазасын / деградациясын немесе амин қышқылдарының деградациясына немесе витаминдер биосинтезіне қатысатын басқа ферменттерді кодтайтын гендердің өкілдігі АҚШ, Малави немесе Америндік тектегі популяциялар арасындағы айтарлықтай айырмашылықтарды көрсетеді.[40]
АҚШ-тың деградациясын кодтайтын ферменттердің саны жоғары глутамин және дәруменге қатысатын ферменттер және липой қышқылы биосинтез; ал Малави және Америндиан популяцияларында глутамат синтазасын кодтайтын ферменттердің саны жоғары және оларда шамадан тыс көрініс бар α-амилаза олардың микробиомында. Жүгеріге бай рационға ие американдық немесе малавиялық популяцияларға қарағанда, АҚШ тұрғындарының құрамында майларға бай диета болғандықтан, диета ішек бактерияларының негізгі анықтаушысы болуы мүмкін.[40]
Әрі қарай жүргізілген зерттеулер Еуропалық және ауылдық африкалық балалар арасындағы микробиотаның құрамындағы үлкен айырмашылықты көрсетті. Бастап балалардың нәжісті бактериялары Флоренция ауылының балаларымен салыстырылды Боулпон жылы Буркина-Фасо. Бұл ауылда тұратын әдеттегі баланың тамақтануы негізінен майлар мен жануарлар ақуыздарынан аз, полисахаридтер мен өсімдік ақуыздарына бай. Еуропалық балалардың нәжісті бактериялары басым болды Firmicutes биологиялық әртүрліліктің айтарлықтай төмендеуін көрсетті, ал Боулпон балаларындағы нәжіс бактериялары басым болды Бактериоидтер. Африка популяцияларындағы биоалуантүрліліктің және ішек флорасының әр түрлі құрамы қалыпты сіңімді емес өсімдік полисахаридтерін қорытуға көмектеседі, сонымен қатар жұқпалы емес ішек ауруларының төмендеуіне әкелуі мүмкін.[45]
Кішігірім масштабта, отбасында қоршаған ортаға әсер етудің көп мөлшерін бөлісу жеке микробиом құрамының күшті анықтаушысы екендігі көрсетілген. Бұл эффект генетикалық әсер етпейді және мәдени тұрғыдан әр түрлі популяцияларда үнемі байқалады.[40]
Тамақтанбау
Тамақтанбаған балаларда сау балалармен салыстырғанда ішек микробиотасы жетілген емес және әртүрлі емес, ал қоректік заттардың жетіспеушілігімен байланысты микробиомның өзгеруі өз кезегінде тамақтанудың патофизиологиялық себебі болуы мүмкін.[46][47] Нашар тамақтанған балаларда, әдетте, патогенді ішек флорасы және т.б. ашытқы олардың аузында және тамағында.[48] Диетаны өзгерту ішек микробиотасының құрамы мен әртүрлілігінің өзгеруіне әкелуі мүмкін.[41]
Нәсіл және этникалық ерекшелік
Американдық ішек жобасы мен адам микробиомы жобасының зерттеушілері он екі микробтар отбасы адамның нәсіліне немесе этникалық ерекшеліктеріне байланысты әр түрлі болатындығын анықтады. Бұл бірлестіктердің күші іріктеудің кішігірім мөлшерімен шектеледі: американдық ішек жобасы 1375 адамнан мәліметтер жинады, олардың 90% -ы ақ түсті.[49] Амстердамдағы қалалық өмірдегі салауатты өмір (HELIUS) зерттеуі нидерландықтардың арғы тегі ішек микробиотасының әртүрлілігімен, ал Оңтүстік Азия мен Суринамдық әртүрліліктің ең төменгі деңгейіне ие болды. Зерттеу нәтижелері бір нәсілге немесе этникалық топқа жататын адамдарда әр түрлі нәсілдік дараларға қарағанда микробиомдар көп болатындығын көрсетті.[49]
Әлеуметтік-экономикалық мәртебе
2020 жылғы жағдай бойынша кем дегенде екі зерттеу жеке тұлғаның зерттеуімен байланысты екенін көрсетті әлеуметтік-экономикалық жағдайы (SES) және олардың ішек микробиоталары. Зерттеу Чикаго SES жоғары аудандарындағы адамдардың микробиоталардың алуан түрлілігі жоғары екендігі анықталды. Жоғары СЭС-тің тұрғындары да көп болды Бактероидтер бактериялар. Сол сияқты, зерттеу егіздер Біріккен Корольдікте жоғары SES-тің ішектің әртүрлілігімен байланысты екендігі анықталды.[49]
Адам нәрестелеріндегі сатып алу
Ішек флорасын құру ересек адамның денсаулығы үшін, сондай-ақ асқазан-ішек жолдарының жұмысы үшін өте маңызды.[50] Адамдарда ересектерге ұқсас ішек флорасы туылғаннан бастап бір-екі жыл ішінде қалыптасады, өйткені микробиоталар ата-анадан балаға жұғу және тамақтан, судан және басқа қоршаған орта көздерінен ауысу арқылы алынады.[51][6]
Дәстүрлі көзқарасы асқазан-ішек жолдары қалыпты ұрық бұл стерильді болып табылады, дегенмен бұл көзқарас соңғы бірнеше жыл ішінде дау тудырды.[52] Жатыр ішілік ортада бактериялар болуы мүмкін деген бірнеше дәлелдер пайда бола бастады. Адамдарда зерттеулер ұрықта микробтық колония пайда болуы мүмкін екенін көрсетті[53] бір зерттеу көрсетілген Лактобакиллус және Бифидобактериялар түрлері плацента биопсиясында болған.[54] Бірнеше кеміргіштерді зерттеу амниотикалық сұйықтықта және плацентада, сондай-ақ стерильді кесар тілігі арқылы туылған нәрестелердің мекониясында бактериялардың болуын көрсетті.[55][56] Тағы бір зерттеуде зерттеушілер жүкті дамбаға бактериялар өсіруді ауызша жолмен жүргізді және ұрпақтардағы бактерияларды анықтады, мүмкін бұл асқазан-ішек жолдары мен амниотикалық сұйықтық арасындағы қан ағымы арқылы.[57] Алайда зерттеушілер бұл жатырішілік бактериялардың көзі, олардың тірі екендігі және олардың рөлі әлі анықталмағанын ескертеді.[58][54]
Туылу кезінде және одан кейін тез арада анадан және қоршаған ортаның бактериялары нәрестенің ішегін колонизациялайды.[6] Бактериялардың нақты көздері толық анықталмаған, бірақ туу каналы, басқа адамдар (ата-аналар, бауырлар, аурухана қызметкерлері), емшек сүті, тамақ және нәресте араласатын жалпы орта болуы мүмкін.[59] Алайда, 2013 жылдан бастап, отарлаудың көп бөлігі анадан туындай ма, жоқ па, белгісіз болып қалады.[6] Туылған нәрестелер кисариялық бөлім сонымен қатар олардың аналарының микрофлорасына ұшырауы мүмкін, бірақ алғашқы әсер қоршаған ортаға, мысалы, ауаға, басқа нәрестелерге және мейірбике қызметкерлеріне әсер етеді, олар тасымалдау үшін вектор ретінде қызмет етеді.[53] Өмірдің бірінші жылы ішек флорасының құрамы негізінен қарапайым және уақыт бойынша көп өзгереді және жеке адамдарда бірдей емес.[6] Бастапқы бактериалды популяция негізінен факультативті анаэробты организмдер; тергеушілер бұл алғашқы колонизаторлар ішектегі оттегінің концентрациясын төмендетеді, бұл өз кезегінде анаэробты бактерияларға жол береді деп санайды. Бактероидтер, Актинобактериялар, және Firmicutes қалыптасу және өркендеу.[6] Емшек сүтімен қоректенетін нәрестелер басым болады бифидобактериялар, мүмкін мазмұнына байланысты өсудің бифидобактериалды факторлары емшек сүтінде және емшек сүтінде бактериялардың сау өсуіне мүмкіндік беретін пребиотикалық компоненттер бар.[54][60] Керісінше, микробиотасы формуламен қоректенеді нәрестелер әртүрлі, олардың саны жоғары Энтеробактериялар, энтерококктар, бифидобактериялар, Бактероидтер, және клостридиялар.[61]
Кесариялық бөлім, антибиотиктер, және қоспаны беру ішектің микробиомының құрамын өзгертуі мүмкін.[54] Антибиотиктермен емделген балаларда тұрақтылық аз, әр түрлі гүлді қауымдастықтар болады.[62] Кесарь тілігі арқылы бактериялардың аналық ұрпақтарға таралуы бұзылған, бұл целиакия, астма және 1 типті қант диабеті сияқты аурулардың қаупін жоғарылату арқылы ұрпақтың денсаулығына әсер етеді.[54] Бұл ішектің сау микробиомының маңыздылығын дәлелдейді. Микробиоманы қалпына келтірудің әртүрлі әдістері зерттелуде, әдетте нәрестені аналық вагинальды мазмұнға және ішке қабылдауға арналған пробиотиктер.[54]
Функциялар
Ішек флорасын зерттеу басталған кезде оның негізгі үш рөлі бар деп ойлады: тікелей қорғаныс патогендер дамытудағы және оны қолдаудағы рөлімен иеленушілердің қорғанысын нығайту ішек эпителийі және антиденелер өндірісін индукциялау, және басқа жолмен тағамға сіңімді емес қосылыстарды метаболиздеу; кейінгі жұмыс иммундық жүйені дамытудағы рөлін анықтады, ал одан әрі жұмыс оның рөліне бағытталған ішек-ми осі.[63]
Қоздырғыштардың тікелей тежелуі
Ішек флорасы қауымдастығы кеңістікті толығымен колонизациялау, қолда бар барлық қоректік заттарды пайдалану және онымен қоректік заттар үшін бәсекеге түсетін жағымсыз ағзаларды тежейтін қосылыстар бөлу арқылы патогендерден қорғауда тікелей рөл атқарады, бұл қосылыстар цитокиндер.[64] Ішек бактерияларының әртүрлі штамдары әртүрлі цитокиндердің пайда болуын тудырады. Цитокиндер - бұл біздің иммундық жүйемізден басталатын химиялық қосылыстар қабыну реакциясы инфекцияларға қарсы. Ішек флорасының бұзылуы сияқты бәсекелес организмдерге мүмкіндік береді Clostridium difficile басқаша жағдайда сақталатыны анықталсын.[64]
Ішектен қорғау және иммундық жүйені дамыту
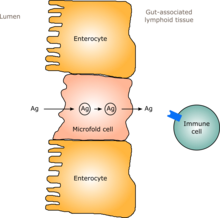
Адамдарда ересек адамға ұқсас ішек флорасы туылғаннан бастап бір-екі жыл ішінде қалыптасады.[6] Ішек флорасы қалыптасқан сайын, ішектің қабығы - ішек эпителийі және ол шығаратын ішектің шырышты қабаты - белгілі бір дәрежеде, сонымен қатар белгілі бір дәрежеде, комменсалистік микроорганизмдерге төзімді, тіпті қолдау көрсететін жолмен дамиды. патогендікке тосқауыл ұсынады.[6] Нақтырақ айтқанда, бокал жасушалары шырышты қабықшаны көбейтетін шырышты қабат қалыңдап, «шырайлы» микроорганизмдер якорьмен қоректене алатын сыртқы шырышты қабатты және тіпті осы организмдер ене алмайтын ішкі қабатты қамтамасыз етеді.[6][7] Сонымен қатар, ішекпен байланысқан лимфоидты тін Ішек эпителийінің бір бөлігін құрайтын және қоздырғыштарды анықтайтын және оларға реакция жасайтын (GALT) ішек флорасы дамып, қалыптасқан уақытта пайда болады және дамиды.[6] Дамыған GALT ішек флорасы түрлеріне төзімді, бірақ басқа микроорганизмдерге төзімді емес.[6] GALT әдетте нәресте ұшырайтын тағамға, сондай-ақ тағамның ас қорыту өнімдеріне және ішек флорасына төзімді болады. метаболиттер (метаболизмнен пайда болған молекулалар) тағамнан түзілген.[6]
Адам иммундық жүйе жасайды цитокиндер иммундық жүйені өзін-өзі қорғау үшін қабынуды тудыруы мүмкін және иммундық реакцияны ұстап тұруы мүмкін гомеостаз және қорлаудан немесе жарақат алғаннан кейін емделуге мүмкіндік беріңіз.[6] Ішек флорасында пайда болатын әр түрлі бактериялық түрлер иммундық жүйені цитокиндерді селективті түрде құруға қабілетті екендігі дәлелденді; Мысалға Bacteroides fragilis және кейбір Клостридия түрлері қабынуға қарсы реакцияны тудырады, ал кейбіреулері жіп тәрізді бактериялар қабыну цитокиндерінің өндірісін жүргізу.[6][65] Ішек флорасы сонымен қатар өндіруді реттей алады антиденелер иммундық жүйе арқылы.[6][66] Осы реттеудің бір функциясы себеп болып табылады В жасушалары сыныпқа ауысу IgA. Көп жағдайда В клеткалары активацияны қажет етеді T көмекші жасушалар тудыру сыныпты ауыстыру; алайда, басқа жолда ішек флорасы пайда болады NF-kB эпителий жасушалары арқылы сигнал беру, нәтижесінде одан әрі сигнал молекулалары бөлінеді.[67] Бұл сигналдық молекулалар В клеткаларымен өзара әрекеттесіп, IgA класына ауысады.[67] IgA - бұл антиденелердің маңызды түрі, ол ішек сияқты шырышты ортада қолданылады. IgA ішектің қауымдастығын әртараптандыруға және қабыну реакциясын тудыратын бактериялардан арылуға көмектесетіні көрсетілген.[68] Сайып келгенде, IgA иесі мен ішек бактериялары арасында сау ортаны сақтайды.[68] Бұл цитокиндер мен антиденелер ішектен тыс, өкпеде және басқа тіндерде әсер етуі мүмкін.[6]
Иммундық жүйені ішек бактерияларының түзілуіне байланысты өзгертуге де болады метаболиттер иммундық жүйенің жасушаларына әсер етуі мүмкін. Мысалға қысқа тізбекті май қышқылдары (SCFA) ішек бактериялары арқылы өндірілуі мүмкін ашыту.[69] SCFAs туа біткен иммундық жасушалар өндірісінің жылдам өсуін ынталандырады нейтрофилдер, базофилдер және эозинофилдер.[69] Бұл жасушалар инфекцияның таралуын шектеуге тырысатын туа біткен иммундық жүйенің бөлігі болып табылады.
Метаболизм
Триптофанның метаболизмі адамның асқазан-ішек микробиотасы () |
Ішек флорасы болмаса, адам ағзасы кейбір сіңірілмеген заттарды пайдалана алмайды көмірсулар ол ішеді, өйткені ішек флорасының кейбір түрлері бар ферменттер адам жасушалары белгілі бір нәрсені бұзуға жетіспейді полисахаридтер.[8] А өсірілген кеміргіштер стерильді қоршаған орта және ішек флорасының жетіспеушілігі 30% көп тамақтану керек калория олардың салмағы әдеттегі аналогтарымен бірдей болу үшін.[8] Адамдар жасай алмайтын көмірсулар дайджест бактериялық көмектің жоқтығына белгілі крахмал, талшық, олигосахаридтер, және қанттар дене сіңіре алмады және сіңіре алмады лактоза жағдайда лактозаға төзбеушілік және қант спирттері, шырыш ішек пен ақуыздар шығарады.[5][8]
Бактериялар өздері ашытатын көмірсуларды айналдырады қысқа тізбекті май қышқылдары деп аталатын ашыту формасы бойынша сахаролитикалық ашыту.[34] Өнімдерге кіреді сірке қышқылы, пропион қышқылы және май қышқылы.[14][34] Бұл материалдарды энергия мен қоректік заттардың негізгі көзін қамтамасыз ететін иесі жасушалар қолдана алады.[34] Газдар (бұл себеп болады метеоризм ) және органикалық қышқылдар, сияқты сүт қышқылы, сонымен қатар ашыту арқылы өндіріледі.[14] Сірке қышқылын қолданады бұлшықет, пропион қышқылы жеңілдетеді бауыр өндірісі ATP, ал май қышқылы ішек жасушаларын энергиямен қамтамасыз етеді.[34]
Ішек флорасы сонымен қатар дәрумендерді синтездейді биотин және фолий және сіңуін жеңілдетеді диеталық минералдар оның ішінде магний, кальций және темір бар.[11][20] Methanobrevibacter smithii бірегей, өйткені ол бактериялардың түрі емес, керісінше оның мүшесі домен Архея, және ең көп метан - адамның асқазан-ішек микробиотасында археологиялық түрлерін шығару.[74]
Ішек микробиотасы организмде өндірілмейтін немесе аз мөлшерде шығарылатын К және В12 витаминдерінің көзі ретінде де қызмет етеді.[75][76]
Фармакомикробиомика
Адам метагеном (яғни жеке тұлғаның генетикалық құрамы және оның денесінде немесе оның ішінде болатын барлық микроорганизмдер) индивидтер арасында айтарлықтай өзгереді.[77][78] Адам ағзасындағы микробтық және вирустық жасушалардың жалпы саны (100 триллионнан астам) өте көп болғандықтан Homo sapiens жасушалар (ондаған триллион),[1 ескерту][77][79] дәрі-дәрмектер мен жеке адамның микробиомасы арасында өзара әрекеттесу мүмкіндігі айтарлықтай, оның ішінде: дәрілік заттардың құрамын өзгертетін дәрілер адамның микробиомасы, дәрілік зат алмасуы препаратты өзгертетін микробтық ферменттер арқылы фармакокинетикалық препараттың клиникалық тиімділігіне әсер ететін және микробтық дәрілік зат алмасуы уыттылық профиль.[77][78][80]
Көмірсулардан басқа, ішек микробиотасы басқаларын метаболиздей алады ксенобиотиктер есірткі сияқты, фитохимиялық заттар және тағамдық токсиканттар. 30-дан астам дәрі-дәрмектің ішек микробиотасы арқылы метаболизденетіні көрсетілген.[81] Дәрілердің микробтық метаболизмі кейде препаратты инактивациялауы мүмкін.[82]
Ішек-ми осі
Ішек-ми осі - бұл арасында болатын биохимиялық сигнал асқазан-ішек жолдары және орталық жүйке жүйесі.[63] Бұл термин интерплейдегі ішек флорасының рөлін қосатын кеңейтілді; кейде «микробиом-ішек-ми осі» термині ішек флорасын қоса парадигмаларды анық сипаттау үшін қолданылады.[63][83][84] Ішек-ми осіне кеңінен анықталған орталық жүйке жүйесі, нейроэндокрин және нейроиммунды жүйелер, соның ішінде гипоталамус-гипофиз-бүйрек үсті осі (HPA осі), симпатикалық және парасимпатикалық қолдар вегетативті жүйке жүйесі оның ішінде ішек жүйке жүйесі, кезбе жүйке және ішек микробиота.[63][84]
A жүйелі шолу 2016 жылдан бастап кейбір коммерциялық қол жетімді штамдарымен жүргізілген клиникаға дейінгі және кішігірім адам сынақтарын зерттеді пробиотикалық бактериялар анықталды және тексерілгендердің арасында Бифидобактериялар және Лактобакиллус тұқымдас (B. longum, B. брев, B. infantis, L. helveticus, L. rhamnosus, L. plantarum, және L. casei ), белгілі біреулерге пайдалы болу үшін ең үлкен әлеуетке ие болды орталық жүйке жүйесінің бұзылуы.[10]
Флора тепе-теңдігінің өзгеруі
Антибиотикті қолданудың әсері
Ішек бактерияларының санын өзгерту, мысалы қабылдау арқылы кең спектрлі антибиотиктер, хосттың денсаулығы мен тағамды қорыту қабілетіне әсер етуі мүмкін.[85] Антибиотиктер тудыруы мүмкін антибиотикпен байланысты диарея (AAD) ішек тікелей, ішек флорасының деңгейін өзгерту немесе мүмкіндік беру патогенді бактериялар өседі.[14] Антибиотиктердің тағы бір зиянды әсері - олардың көбеюі антибиотиктерге төзімді бактериялар оларды қолданғаннан кейін табылған, олар иесін басып алған кезде антибиотиктермен емделуі қиын аурулар тудырады.[85]
Ішек флорасының саны мен түрлерін өзгерту организмнің көмірсулар мен метаболизмді ашыту қабілетін төмендетуі мүмкін өт қышқылдар тудыруы мүмкін диарея. Бөлінбейтін көмірсулар суды көп сіңіріп, нәжісті тудыруы мүмкін, немесе ішек флорасында өндірілетін SCFA жетіспеушілігі диареяны тудыруы мүмкін.[14]
Жергілікті бактериялардың деңгейінің төмендеуі олардың зиянды түрлерінің көбеюіне кедергі келтіреді C. difficile және Сальмонелла кедугу және бұл түрлер қолдан шығып кетуі мүмкін, бірақ олардың өсуі кездейсоқ болуы мүмкін және диареяның нақты себебі емес.[11][14][85] Дамып келе жатқан C. difficile инфекциясын емдеу протоколдары донорлық нәжісті нәжіс микробиотасы трансплантациясын қамтиды. (қараңыз Нәжісті трансплантациялау ). Емдеудің алғашқы есептері сәттіліктің 90% -ын сипаттайды, оның жанама әсерлері аз. Тиімділігі бактероидтық бактерия тепе-теңдігін қалпына келтіру және бактериялардың фирмалық кластары нәтижесінде пайда болады деп болжануда.[86]
Ішек флорасының құрамы ауыр аурулар кезінде де өзгереді, бұл тек антибиотикті қолдануға ғана емес, сонымен қатар факторларға байланысты ишемия ішектің, тамақтанбаудың және иммундық ымыраға келу. Осыдан туындаған жағымсыз әсерлер қызығушылық тудырды ас қорыту жолдарын селективті зарарсыздандыру (SDD), тек патогендік бактерияларды жоюға және сау бактерияларды қалпына келтіруге мүмкіндік беретін емдеу әдісі.[87]
Антибиотиктер популяцияны өзгертеді асқазан-ішек жолдары (GI) микробиота, қауымдастық ішіндегі метаболикалық өзара әрекеттесуді өзгерте алады, көмірсулар қолдану арқылы калориялы тұтынуды өзгертеді және глобальды түрде метаболикалық, гормондық және иммундық гомеостазға әсер етеді.[88]
Құрамында пробиотиктерді қабылдау туралы дәлелдер бар Лактобакиллус түрлері антибиотикпен байланысты диареяның алдын алуға және пробиотиктерді қабылдауға көмектеседі Сахаромицес (мысалы, Saccharomyces boulardii ) алдын алуға көмектеседі Clostridium difficile жүйелік антибиотиктік емнен кейінгі инфекция.[89]
Жүктілік
Әйелдердің ішек микробиотасы жүктіліктің жоғарылауына байланысты өзгереді, және өзгерген өзгерістерге ұқсас метаболикалық синдромдар қант диабеті сияқты. Ішек флорасының өзгеруі жаман әсер етпейді. Жаңа туған нәрестенің ішек биотасы ананың бірінші триместріндегі үлгілерге ұқсайды. Флораның әртүрлілігі бірінші триместрден үшінші триместрге дейін азаяды, өйткені кейбір түрлердің саны өседі.[54][90]
Пробиотиктер, пребиотиктер, синбиотиктер және фарбиотиктер
Пробиотиктер болып табылады микроорганизмдер тұтыну кезінде денсаулыққа пайда әкеледі деп саналады.[91][92] Ішек флорасына қатысты, пребиотиктер әдетте сіңімді емес, талшық -ның жоғарғы бөлігі арқылы сіңірілмеген өтетін қосылыстар асқазан-ішек жолдары сияқты әрекет ету арқылы тиімді ішек флорасының өсуін немесе белсенділігін ынталандырады субстрат олар үшін.[34][93]
Синбиотиктер сілтеме жасайды тамақ ингредиенттері немесе тағамдық қоспалар түрінде пробиотиктер мен пребиотиктерді біріктіру синергизм.[94]
«Фармациотиктер» термині әр түрлі тәсілдермен қолданылады: фармацевтикалық құрамдар (есірткі ретінде нормативтік мақұлдау ала алатын стандартталған өндіріс) пробиотиктер, пребиотиктер, немесе синбиотиктер;[95] генетикалық инженерияланған немесе басқа жолмен оңтайландырылған пробиотиктер (сақтау мерзімі, ас қорыту жолында тіршілік ету және т.б.);[96] және ішек флорасы метаболизмінің табиғи өнімдері (витаминдер және т.б.).[97]
Кейбір пробиотикалық штамдармен бактерияларды емдеу тиімді болуы мүмкін екендігі туралы бірнеше дәлел бар тітіркенген ішек синдромы және созылмалы идиопатиялық іш қату. Симптомдардың төмендеуіне алып келетін организмдерге мыналар кірді:
- Enterococcus faecium
- Lactobacillus plantarum
- Lactobacillus rhamnosus
- Propionibacterium freudenreichii
- Bifidobacterium breve
- Lactobacillus reuteri
- Lactobacillus salivarius
- Bifidobacterium infantis
- Streptococcus thermophilus[98][99][100]
Зерттеу
Антибиотикке жатпайтын дәрі-дәрмектер адамның ішегімен байланысқан бактерияларға әсер етуі мүмкін еместігіне тесттер жүргізді in vitro сатылатын 1000-нан астам дәрі-дәрмектерге 40 ішек бактерия штамдарына қарсы талдау жүргізу, бұл дәрілердің 24% -ы бактерия штамдарының кем дегенде біреуінің өсуін тежейтіндігін көрсетті.[101]
Аурудағы рөлі
Ас қорыту жолындағы бактериялар ауруға әр түрлі әсер етуі және әсер етуі мүмкін. Кейбір бактериялардың болуы немесе олардың көп болуы қабыну бұзылуларына ықпал етуі мүмкін ішектің қабыну ауруы.[11] Сонымен қатар, ішек флорасының кейбір мүшелерінен метаболиттер иелердің сигнал беру жолдарына әсер етуі мүмкін, мысалы, бұзылуларға ықпал етеді семіздік және ішектің қатерлі ісігі.[11] Сонымен қатар, ішектің бұзылуы жағдайында эпителий, ішек флорасы компоненттерінің басқа хост бөлімдеріне енуіне әкелуі мүмкін сепсис.[11]
Жаралар
Хеликобактерия инфекция бактериялар асқазанның эпителиалды қабығына еніп, содан кейін ан тудыратын кезде асқазан жарасының пайда болуын бастауы мүмкін қабыну фагоцитотикалық реакциясы.[102] Өз кезегінде қабыну париетальды жасушаларды зақымдайды, олар асқазанға көп мөлшерде тұз қышқылын шығарады және қорғаныш шырышты аз шығарады.[103] Асқазан қабығының жарақаты, әкеледі жаралар, асқазан қышқылы жасушалардың қорғаныс қасиеттерін асырып, эндогенді тежейтін кезде дамиды простагландин синтез, шырыш пен бикарбонаттың бөлінуін азайтады, шырышты қан ағынын азайтады және жарақатқа төзімділікті төмендетеді.[103] Асқазан қабатының қорғаныш қасиеттерінің төмендеуі одан әрі жарақаттануға және асқазан қышқылы, пепсин және өт тұздарының әсерінен жараның пайда болуына әсер етеді.[102][103]
Ішектің перфорациясы
Қалыпты-коменсалды бактериялар егер олар ішек жолынан шығып кетсе, хостқа зиян тигізуі мүмкін.[6][7] Транслокация бұл бактериялар ішек арқылы шыққан кезде пайда болады шырышты жабыны, әр түрлі ауруларда пайда болуы мүмкін.[7] Егер ішек тесілген болса, бактериялар еніп кетеді интерстиций, өлімге әкелуі мүмкін инфекция.[4]:715
Ішектің қабыну аурулары
Екі негізгі түрі ішектің қабыну аурулары, Крон ауруы және жаралы колит, болып табылады созылмалы ішектің қабыну бұзылыстары; бұл аурулардың себептері белгісіз және бұл жағдайда ішек флорасы мен оның иесімен байланысы туралы мәселелер туындаған.[9][104][105][106] Сонымен қатар, ішек-флораның ішек-ми осімен өзара әрекеттесуі IBD-де маңызды рөл атқарады, физиологиялық стресс арқылы гипоталамус-гипофиз-бүйрек үсті осі ішек эпителийіне және ішек флорасына өзгерістер енгізу, өз кезегінде факторларды және метаболиттерді босатып, сигнал беруді бастайды ішек жүйке жүйесі және кезбе жүйке.[3]
Ішек флорасының әртүрлілігі ішектің қабыну аурулары бар адамдарда сау адамдармен салыстырғанда айтарлықтай азаятын көрінеді; қосымша, жаралы колитпен ауыратын адамдарда протеобактериялар мен актинобактериялар басым болады; Кронмен ауыратын адамдарда, Enterococcus faecium and several Proteobacteria appear to be over-represented.[3]
There is reasonable evidence that correcting gut flora imbalances by taking probiotics with Лактобактериялар және Bifidobacteria can reduce visceral pain and gut inflammation in IBD.[89]
Irritable bowel syndrome
Irritable bowel syndrome is a result of stress and chronic activation of the HPA axis; its symptoms include abdominal pain, changes in bowel movements, and an increase in proinflammatory cytokines. Overall, studies have found that the luminal and mucosal microbiota are changed in irritable bowel syndrome individuals, and these changes can relate to the type of irritation such as diarrhea or іш қату. Also, there is a decrease in the diversity of the microbiome with low levels of fecal Lactobacilli and Bifidobacteria, high levels of facultative анаэробты бактериялар сияқты Ішек таяқшасы, and increased ratios of Firmicutes: Bacteroidetes.[84]
Other inflammatory or autoimmune conditions
Аллергия, астма, және қант диабеті болып табылады аутоиммунды және inflammatory disorders of unknown cause, but have been linked to imbalances in the gut flora and its relationship with the host.[9] As of 2016 it was not clear if changes to the gut flora cause these auto-immune and inflammatory disorders or are a product of or adaptation to them.[9][107]
Демікпе
With asthma, two hypotheses have been posed to explain its rising prevalence in the developed world. The гигиеналық гипотеза posits that children in the developed world are not exposed to enough microbes and thus may contain lower prevalence of specific bacterial taxa that play protective roles.[108] The second hypothesis focuses on the Western pattern diet, which lacks дәнді дақылдар және талшық and has an overabundance of қарапайым қанттар.[9] Both hypotheses converge on the role of short-chain fatty acids (SCFAs) in иммуномодуляция. These bacterial fermentation metabolites are involved in immune signalling that prevents the triggering of asthma and lower SCFA levels are associated with the disease.[108][109] Lacking protective genera such as Lachnospira, Вейлонелла, Ротия және Faecalibacterium has been linked to reduced SCFA levels.[108] Further, SCFAs are the product of bacterial fermentation of fiber, which is low in the Western pattern diet.[9][109] SCFAs offer a link between gut flora and immune disorders, and as of 2016, this was an active area of research.[9] Similar hypotheses have also been posited for the rise of food and other allergies.[110]
1 типті қант диабеті
The connection between the gut microbiota and 1 типті қант диабеті has also been linked to SCFAs, such as бутират and acetate. Diets yielding butyrate and acetate from bacterial fermentation show increased Тобл өрнек.[111] Тобл жасушалар downregulate эффекторлы Т жасушалары, which in turn reduces the қабыну реакциясы ішекте.[112] Butyrate is an energy source for colon cells. butyrate-yielding diets thus decrease gut permeability by providing sufficient energy for the formation of тығыз өткелдер.[113] Additionally, butyrate has also been shown to decrease insulin resistance, suggesting gut communities low in butyrate-producing microbes may increase chances of acquiring қант диабеті 2 тип.[114] Butyrate-yielding diets may also have potential тік ішек рагы suppression effects.[113]
Obesity and metabolic syndrome
The gut flora has also been implicated in obesity and метаболикалық синдром due to the key role it plays in the digestive process; the Western pattern diet appears to drive and maintain changes in the gut flora that in turn change how much energy is derived from food and how that energy is used.[106][115] One aspect of a дұрыс тамақтану that is often lacking in the Western-pattern diet is fiber and other complex carbohydrates that a healthy gut flora require flourishing; changes to gut flora in response to a Western-pattern diet appear to increase the amount of energy generated by the gut flora which may contribute to obesity and metabolic syndrome.[89] There is also evidence that microbiota influence eating behaviours based on the preferences of the microbiota, which can lead to the host consuming more food eventually resulting in obesity. It has generally been observed that with higher gut microbiome diversity, the microbiota will spend energy and resources on competing with other microbiota and less on manipulating the host. The opposite is seen with lower gut microbiome diversity, and these microbiotas may work together to create host food cravings.[41]
Additionally, the liver plays a dominant role in қандағы глюкоза homeostasis by maintaining a balance between the uptake and storage of glucose through the metabolic pathways of glycogenesis және глюконеогенез. Intestinal lipids regulate glucose homeostasis involving a gut-brain-liver axis. The direct administration of lipids into the upper intestine increases the long chain fatty acyl-coenzyme A (LCFA-CoA) levels in the upper intestines and suppresses glucose production even under subdiaphragmatic ваготомия or gut vagal deafferentation. This interrupts the neural connection between the brain and the gut and blocks the upper intestinal lipids' ability to inhibit glucose production. The gut-brain-liver axis and gut microbiota composition can regulate the glucose homeostasis in the liver and provide potential therapeutic methods to treat obesity and diabetes.[116]
Just as gut flora can function in a feedback loop that can drive the development of obesity, there is evidence that restricting intake of calories (i.e., диета ) can drive changes to the composition of the gut flora.[106]
Бауыр ауруы
As the liver is fed directly by the портал венасы, whatever crosses the intestinal epithelium and the intestinal mucosal barrier enters the liver, as do cytokines generated there.[117] Dysbiosis in the gut flora has been linked with the development of цирроз және алкогольсіз бауыр майлы ауруы.[117]
Қатерлі ісік
Some genera of bacteria, such as Бактероидтер және Клостридий, have been associated with an increase in ісік growth rate, while other genera, such as Лактобакиллус және Bifidobacteria, are known to prevent tumor formation.[11] As of December 2017 there was preliminary and indirect evidence that gut microbiota might mediate response to PD-1 inhibitors; the mechanism was unknown.[118]
Нейропсихиатриялық
Interest in the relationship between gut flora and neuropsychiatric issues was sparked by a 2004 study showing that germ-free mice showed an exaggerated HPA axis response to stress compared to non-GF laboratory mice.[63] As of January 2016, most of the work that has been done on the role of gut flora in the gut-brain axis had been conducted in animals, or characterizing the various neuroactive compounds that gut flora can produce, and studies with humans measuring differences between people with various psychiatric and neurological differences, or changes to gut flora in response to stress, or measuring effects of various probiotics (dubbed "psychobiotics in this context), had generally been small and could not be generalized; whether changes to gut flora are a result of disease, a cause of disease, or both in any number of possible feedback loops in the gut-brain axis, remained unclear.[63][89]
A systematic review from 2016 examined the preclinical and small human trials that have been conducted with certain commercially available strains of probiotic bacteria and found that among those tested, the genera Бифидобактериялар және Лактобакиллус (B. longum, B. breve, B. infantis, L. helveticus, L. rhamnosus, L. plantarum, және L. casei) had the most potential to be useful for certain central nervous system disorders.[10]
Басқа жануарлар
The composition of the human gut microbiome is similar to that of the other great apes. However, humans’ gut biota has decreased in diversity and changed in composition since our evolutionary split from Пан.[119] Humans display increases in Bacteroidetes, a bacterial phylum associated with diets high in animal protein and fat, and decreases in Methanobrevibacter and Fibrobacter, groups that ferment complex plant polysaccharides.[119] These changes are the result of the combined dietary, genetic, and cultural changes humans have undergone since evolutionary divergence from Пан.
In addition to humans and vertebrates, some insects also possess complex and diverse gut microbiota that play key nutritional roles.[120] Microbial communities associated with termites can constitute a majority of the weight of the individuals and perform important roles in the digestion of лигноцеллюлоза және nitrogen fixation.[121] These communities are host-specific, and closely related insect species share comparable similarities in gut microbiota composition.[122][123] Жылы тарақандар, gut microbiota have been shown to assemble in a deterministic fashion, irrespective of the егу;[124] the reason for this host-specific assembly remains unclear. Bacterial communities associated with insects like termites and cockroaches are determined by a combination of forces, primarily diet, but there is some indication that host филогения may also be playing a role in the selection of lineages.[122][123]
For more than 51 years it has been known that the administration of low doses of antibacterial agents promotes the growth of farm animals to increase weight gain.[88]
In a study carried out on тышқандар қатынасы Firmicutes және Лахноспирация was significantly elevated in animals treated with subtherapeutic doses of different antibiotics. By analyzing the caloric content of faeces and the concentration of small chain fatty acids (SCFAs) in the GI tract, it was concluded that the changes in the composition of microbiota lead to an increased capacity to extract calories from otherwise indigestible constituents, and to an increased production of SCFAs. These findings provide evidence that antibiotics perturb not only the composition of the GI microbiome but also its metabolic capabilities, specifically with respect to SCFAs.[88]
Сондай-ақ қараңыз
- Colonisation resistance
- List of human flora
- Әйелдердің төменгі репродуктивті трактінің микробиотикалық түрлерінің тізімі
- Тері флорасы
- Веротоксин шығарады Ішек таяқшасы
Ескертулер
Әдебиеттер тізімі
- ^ Moszak, M; Szulińska, M; Bogdański, P (15 April 2020). "You Are What You Eat-The Relationship between Diet, Microbiota, and Metabolic Disorders-A Review". Қоректік заттар. 12 (4): 1096. дои:10.3390/nu12041096. PMID 32326604. S2CID 216108564.
- ^ Segata, N; Boernigen, D; Tickle, TL; Morgan, XC; Garrett, WS; Huttenhower, C (14 May 2013). "Computational meta'omics for microbial community studies". Молекулалық жүйелер биологиясы. 9: 666. дои:10.1038/msb.2013.22. PMID 23670539.
- ^ а б c Saxena, R.; Sharma, V.K (2016). "A Metagenomic Insight Into the Human Microbiome: Its Implications in Health and Disease". In D. Kumar; S. Antonarakis (eds.). Medical and Health Genomics. Elsevier Science. б. 117. дои:10.1016/B978-0-12-420196-5.00009-5. ISBN 978-0-12-799922-7.
- ^ а б c г. e f ж сағ мен j к л Шервуд, Линда; Уилли, Джоанн; Вулвертон, Кристофер (2013). Прескоттың микробиологиясы (9-шы басылым). New York: McGraw Hill. 713-21 бет. ISBN 9780073402406. OCLC 886600661.
- ^ а б c г. e Quigley, E. M (2013). "Gut bacteria in health and disease". Гастроэнтерология және гепатология. 9 (9): 560–9. PMC 3983973. PMID 24729765.
- ^ а б c г. e f ж сағ мен j к л м n o б q Sommer, Felix; Bäckhed, Fredrik (2013). "The gut microbiota — masters of host development and physiology". Микробиологияның табиғаты туралы шолулар. 11 (4): 227–38. дои:10.1038/nrmicro2974. PMID 23435359. S2CID 22798964.
- ^ а б c г. Faderl, Martin; Noti, Mario; Corazza, Nadia; Mueller, Christoph (2015). "Keeping bugs in check: The mucus layer as a critical component in maintaining intestinal homeostasis". IUBMB Life. 67 (4): 275–85. дои:10.1002/iub.1374. PMID 25914114. S2CID 25878594.
- ^ а б c г. e f Clarke, Gerard; Stilling, Roman M; Kennedy, Paul J; Stanton, Catherine; Cryan, John F; Dinan, Timothy G (2014). "Minireview: Gut Microbiota: The Neglected Endocrine Organ". Молекулалық эндокринология. 28 (8): 1221–38. дои:10.1210/me.2014-1108. PMC 5414803. PMID 24892638.
- ^ а б c г. e f ж сағ Shen, Sj; Wong, Connie HY (2016). "Bugging inflammation: Role of the gut microbiota". Clinical & Translational Immunology. 5 (4): e72. дои:10.1038/cti.2016.12. PMC 4855262. PMID 27195115.
- ^ а б c Wang, Huiying; Lee, In-Seon; Braun, Christoph; Enck, Paul (2016). "Effect of Probiotics on Central Nervous System Functions in Animals and Humans: A Systematic Review". Нейрогастроэнтерология және қозғалғыштық журналы. 22 (4): 589–605. дои:10.5056/jnm16018. PMC 5056568. PMID 27413138.
- ^ а б c г. e f ж сағ мен j к л м n o б Guarner, F; Malagelada, J (2003). «Денсаулық пен аурудағы ішек флорасы». Лансет. 361 (9356): 512–19. дои:10.1016 / S0140-6736 (03) 12489-0. PMID 12583961. S2CID 38767655.
- ^ а б c г. e f Sears, Cynthia L. (2005). "A dynamic partnership: Celebrating our gut flora". Anaerobe. 11 (5): 247–51. дои:10.1016 / j.anaerobe.2005.05.001. PMID 16701579.
- ^ Shapira, Michael (2016-07-01). "Gut Microbiotas and Host Evolution: Scaling Up Symbiosis". Экология мен эволюция тенденциялары. 31 (7): 539–549. дои:10.1016/j.tree.2016.03.006. ISSN 0169-5347. PMID 27039196.
- ^ а б c г. e f ж сағ мен j Beaugerie, Laurent; Petit, Jean-Claude (2004). "Antibiotic-associated diarrhoea". Best Practice & Research Clinical Gastroenterology. 18 (2): 337–52. дои:10.1016 / j.bpg.2003.10.002. PMID 15123074.
- ^ Stephen, A. M.; Cummings, J. H. (1980). "The Microbial Contribution to Human Faecal Mass". Медициналық микробиология журналы. 13 (1): 45–56. дои:10.1099/00222615-13-1-45. PMID 7359576.
- ^ Lozupone, Catherine A.; Stombaugh, Jesse I.; Gordon, Jeffrey I.; Jansson, Janet K.; Knight, Rob (2012). "Diversity, stability and resilience of the human gut microbiota". Табиғат. 489 (7415): 220–30. Бибкод:2012Natur.489..220L. дои:10.1038/nature11550. PMC 3577372. PMID 22972295.
- ^ Qin, Junjie; Li, Ruiqiang; Raes, Jeroen; Арумугам, Маниможиян; Burgdorf, Kristoffer Solvsten; Manichanh, Chaysavanh; Nielsen, Trine; Понс, Николас; Левенес, Флоренция; Yamada, Takuji; Менде, Даниэль Р .; Li, Junhua; Xu, Junming; Li, Shaochuan; Li, Dongfang; Cao, Jianjun; Ван, Бо; Liang, Huiqing; Zheng, Huisong; Xie, Yinlong; Түрт, Джульен; Lepage, Patricia; Bertalan, Marcelo; Batto, Jean-Michel; Hansen, Torben; Le Paslier, Denis; Linneberg, Allan; Nielsen, H. Bjørn; Pelletier, Eric; Renault, Pierre (2010). "A human gut microbial gene catalogue established by metagenomic sequencing". Табиғат. 464 (7285): 59–65. Бибкод:2010Natur.464...59.. дои:10.1038/nature08821. PMC 3779803. PMID 20203603.
- ^ Shanahan, Fergus (2002). "The host–microbe interface within the gut". Best Practice & Research Clinical Gastroenterology. 16 (6): 915–31. дои:10.1053/bega.2002.0342. PMID 12473298.
- ^ Түрт, Джульен; Mondot, Stanislas; Левенес, Флоренция; Pelletier, Eric; Caron, Christophe; Furet, Jean-Pierre; Ugarte, Edgardo; Muñoz-Tamayo, Rafael; Paslier, Denis L. E.; Nalin, Renaud; Dore, Joel; Leclerc, Marion (2009). "Towards the human intestinal microbiota phylogenetic core". Environmental Microbiology. 11 (10): 2574–84. дои:10.1111/j.1462-2920.2009.01982.x. PMID 19601958.
- ^ а б O'Hara, Ann M; Shanahan, Fergus (2006). "The gut flora as a forgotten organ". EMBO есептері. 7 (7): 688–93. дои:10.1038/sj.embor.7400731. PMC 1500832. PMID 16819463.
- ^ Khanna, Sahil; Tosh, Pritish K (2014). "A Clinician's Primer on the Role of the Microbiome in Human Health and Disease". Mayo клиникасының материалдары. 89 (1): 107–14. дои:10.1016/j.mayocp.2013.10.011. PMID 24388028.
- ^ а б Cui, Lijia; Morris, Alison; Ghedin, Elodie (2013). "The human mycobiome in health and disease". Геномдық медицина. 5 (7): 63. дои:10.1186/gm467. PMC 3978422. PMID 23899327.
- ^ Erdogan, Askin; Rao, Satish S. C (2015). "Small Intestinal Fungal Overgrowth". Гастроэнтерология туралы ағымдағы есептер. 17 (4): 16. дои:10.1007/s11894-015-0436-2. PMID 25786900. S2CID 3098136.
- ^ Bello, Maria G. Dominguez; Knight, Rob; Gilbert, Jack A.; Blaser, Martin J. (4 October 2018). "Preserving microbial diversity". Ғылым. 362 (6410): 33–34. Бибкод:2018Sci...362...33B. дои:10.1126/science.aau8816. PMID 30287652. S2CID 52919917.
- ^ а б Арумугам, Маниможиян; Raes, Jeroen; Pelletier, Eric; Le Paslier, Denis; Yamada, Takuji; Менде, Даниэль Р .; Fernandes, Gabriel R.; Түрт, Джульен; Bruls, Thomas; Batto, Jean-Michel; Bertalan, Marcelo; Borruel, Natalia; Casellas, Francesc; Fernandez, Leyden; Gautier, Laurent; Hansen, Torben; Hattori, Masahira; Хаяши, Тецуя; Kleerebezem, Michiel; Kurokawa, Ken; Leclerc, Marion; Левенес, Флоренция; Manichanh, Chaysavanh; Nielsen, H. Bjørn; Nielsen, Trine; Понс, Николас; Poulain, Julie; Qin, Junjie; Sicheritz-Ponten, Thomas; Tims, Sebastian (2011). "Enterotypes of the human gut microbiome". Табиғат. 473 (7346): 174–80. Бибкод:2011Natur.473..174.. дои:10.1038/nature09944. PMC 3728647. PMID 21508958.
- ^ а б Wu, G. D.; Chen, J.; Гофман, С .; Bittinger, K.; Chen, Y.-Y.; Keilbaugh, S. A.; Bewtra, M.; Knights, D.; Walters, W. A.; Knight, R.; Sinha, R.; Gilroy, E.; Gupta, K.; Baldassano, R.; Nessel, L.; Ли, Х .; Bushman, F. D.; Lewis, J. D. (2011). "Linking Long-Term Dietary Patterns with Gut Microbial Enterotypes". Ғылым. 334 (6052): 105–08. Бибкод:2011Sci ... 334..105W. дои:10.1126 / ғылым.1208344. PMC 3368382. PMID 21885731.
- ^ Zimmer, Carl (April 20, 2011). "Bacteria Divide People Into 3 Types, Scientists Say". The New York Times. Алынған 21 сәуір, 2011.
a group of scientists now report just three distinct ecosystems in the guts of people they have studied.
- ^ Knights, Dan; Ward, Tonya; McKinlay, Christopher; Miller, Hannah; Gonzalez, Antonio; McDonald, Daniel; Knight, Rob (8 October 2014). "Rethinking "Enterotypes"". Cell Host & Microbe. 16 (4): 433–37. дои:10.1016/j.chom.2014.09.013. PMC 5558460. PMID 25299329.
- ^ Kenneth Todar (2012). "The Normal Bacterial Flora of Humans". Тодардың бактериологияның онлайн оқулығы. Алынған 25 маусым, 2016.
- ^ Quigley, Eamonn M.M; Quera, Rodrigo (2006). "Small Intestinal Bacterial Overgrowth: Roles of Antibiotics, Prebiotics, and Probiotics". Гастроэнтерология. 130 (2): S78–90. дои:10.1053/j.gastro.2005.11.046. PMID 16473077. S2CID 16904501.
- ^ Adams, M. R.; Moss, M. O. (2007). Азық-түлік микробиологиясы. дои:10.1039/9781847557940. ISBN 978-0-85404-284-5.
- ^ а б Глазго университеті. 2005 ж. Ішектің қалыпты флорасы. Веб-архив арқылы қол жетімді. 22 мамырда қол жеткізілді
- ^ а б Steinhoff, U (2005). "Who controls the crowd? New findings and old questions about the intestinal microflora". Иммунологиялық хаттар. 99 (1): 12–16. дои:10.1016/j.imlet.2004.12.013. PMID 15894105.
- ^ а б c г. e f Gibson, Glenn R (2004). "Fibre and effects on probiotics (the prebiotic concept)". Clinical Nutrition Supplements. 1 (2): 25–31. дои:10.1016/j.clnu.2004.09.005.
- ^ Miquel, S; Martín, R; Rossi, O; Bermúdez-Humarán, LG; Chatel, JM; Sokol, H; Томас, М; Wells, JM; Langella, P (2013). "Faecalibacterium prausnitzii and human intestinal health". Микробиологиядағы қазіргі пікір. 16 (3): 255–61. дои:10.1016/j.mib.2013.06.003. PMID 23831042.
- ^ Ley, Ruth E (2010). "Obesity and the human microbiome". Гастроэнтерологиядағы қазіргі пікір. 26 (1): 5–11. дои:10.1097/MOG.0b013e328333d751. PMID 19901833. S2CID 23329156.
- ^ Nash, Andrea K; Auchtung, Thomas A; Wong, Matthew C; Smith, Daniel P; Gesell, Jonathan R; Ross, Matthew C; Stewart, Christopher J; Metcalf, Ginger A; Muzny, Donna M; Gibbs, Richard A; Ajami, Nadim J; Petrosino, Joseph F (2017). "The gut mycobiome of the Human Microbiome Project healthy cohort". Микробиома. 5 (1): 153. дои:10.1186/s40168-017-0373-4. PMC 5702186. PMID 29178920.
- ^ Scarpellini, Emidio; Ianiro, Gianluca; Attili, Fabia; Bassanelli, Chiara; De Santis, Adriano; Gasbarrini, Antonio (2015). "The human gut microbiota and virome: Potential therapeutic implications". Ас қорыту және бауыр аурулары. 47 (12): 1007–12. дои:10.1016/j.dld.2015.07.008. PMID 26257129.
- ^ Gerritsen, Jacoline; Smidt, Hauke; Rijkers, Ger; de Vos, Willem (27 May 2011). "Intestinal microbiota in human health and disease: the impact of probiotics". Genes & Nutrition. 6 (3): 209–40. дои:10.1007/s12263-011-0229-7. PMC 3145058. PMID 21617937.
- ^ а б c г. e f Yatsunenko, T.; Rey, F. E.; Manary, M. J.; Trehan, I.; Dominguez-Bello, M. G.; Contreras, M.; Magris, M.; Hidalgo, G.; Baldassano, R. N.; Anokhin, A. P.; Хит, А. С .; Warner, B.; Reeder, J.; Kuczynski, J.; Caporaso, J. G.; Lozupone, C. A.; Лаубер, С .; Clemente, J. C.; Knights, D.; Knight, R.; Gordon, J. I. (2012). "Human gut microbiome viewed across age and geography". Табиғат. 486 (7402): 222–27. Бибкод:2012Natur.486..222Y. дои:10.1038/nature11053. PMC 3376388. PMID 22699611.
- ^ а б c Алкок, Джо; Maley, Carlo C; Aktipis, C. Athena (2014). "Is eating behavior manipulated by the gastrointestinal microbiota? Evolutionary pressures and potential mechanisms". БиоЭсселер. 36 (10): 940–9. дои:10.1002/bies.201400071. PMC 4270213. PMID 25103109.
- ^ Yeh, Ming-Chin; Glick-Bauer, Marian (November 2014). "The Health Advantage of a Vegan Diet: Exploring the Gut Microbiota Connection". Қоректік заттар. 6 (11): 4822–4838. дои:10.3390/nu6114822. PMC 4245565. PMID 25365383.
- ^ а б David, Lawrence A.; Maurice, Corinne F.; Carmody, Rachel N.; Gootenberg, David B.; Button, Julie E.; Wolfe, Benjamin E.; Ling, Alisha V.; Devlin, A. Sloan; Varma, Yug; Fischbach, Michael A.; Biddinger, Sudha B.; Dutton, Rachel J.; Turnbaugh, Peter J. (11 December 2013). "Diet rapidly and reproducibly alters the human gut microbiome". Табиғат. 505 (7484): 559–563. дои:10.1038/nature12820. PMC 3957428. PMID 24336217.
- ^ Jeffery, Ian; O'Toole, Paul (17 January 2013). "Diet-Microbiota Interactions and Their Implications for Healthy Living". Қоректік заттар. 5 (1): 234–252. дои:10.3390/nu5010234. PMC 3571646. PMID 23344252.
- ^ De Filippo, C; Cavalieri, D; Di Paola, M; Ramazzotti, M; Poullet, J. B; Massart, S; Collini, S; Pieraccini, G; Lionetti, P (2010). "Impact of diet in shaping gut microbiota revealed by a comparative study in children from Europe and rural Africa". Ұлттық ғылым академиясының материалдары. 107 (33): 14691–6. Бибкод:2010PNAS..10714691D. дои:10.1073 / pnas.1005963107. PMC 2930426. PMID 20679230.
- ^ Jonkers, Daisy M.A.E. (2016). "Microbial perturbations and modulation in conditions associated with malnutrition and malabsorption". Best Practice & Research Clinical Gastroenterology. 30 (2): 161–72. дои:10.1016/j.bpg.2016.02.006. PMID 27086883.
- ^ Million, Matthieu; Diallo, Aldiouma; Raoult, Didier (May 2017). "Gut microbiota and malnutrition". Microbial Pathogenesis. 106: 127–138. дои:10.1016/j.micpath.2016.02.003. PMID 26853753.
- ^ Rytter, Maren Johanne Heilskov; Kolte, Lilian; Briend, André; Friis, Henrik; Christensen, Vibeke Brix (2014). "The Immune System in Children with Malnutrition—A Systematic Review". PLOS ONE. 9 (8): e105017. Бибкод:2014PLoSO...9j5017R. дои:10.1371/journal.pone.0105017. PMC 4143239. PMID 25153531.
- ^ а б c Renson, Audrey; Herd, Pamela; Dowd, Jennifer B. (2020). "Sick Individuals and Sick (Microbial) Populations: Challenges in Epidemiology and the Microbiome". Қоғамдық денсаулық сақтаудың жыл сайынғы шолуы. 41: 63–80. дои:10.1146/annurev-publhealth-040119-094423. PMID 31635533.
- ^ Turroni, Francesca; Peano, Clelia; Pass, Daniel A; Foroni, Elena; Severgnini, Marco; Claesson, Marcus J; Kerr, Colm; Hourihane, Jonathan; Murray, Deirdre; Fuligni, Fabio; Gueimonde, Miguel; Margolles, Abelardo; De Bellis, Gianluca; o'Toole, Paul W; Van Sinderen, Douwe; Marchesi, Julian R; Ventura, Marco (2012). "Diversity of Bifidobacteria within the Infant Gut Microbiota". PLOS ONE. 7 (5): e36957. Бибкод:2012PLoSO...736957T. дои:10.1371/journal.pone.0036957. PMC 3350489. PMID 22606315.
- ^ Davenport, Emily R.; Sanders, Jon G.; Song, Se Jin; Amato, Katherine R.; Clark, Andrew G.; Knight, Rob (2017-12-27). "The human microbiome in evolution". BMC биологиясы. 15 (1): 127. дои:10.1186/s12915-017-0454-7. ISSN 1741-7007. PMC 5744394. PMID 29282061.
- ^ Perez-Muñoz, Maria Elisa; Arrieta, Marie-Claire; Ramer-Tait, Amanda E; Walter, Jens (2017). "A critical assessment of the 'sterile womb' and 'in utero colonization' hypotheses: Implications for research on the pioneer infant microbiome". Микробиома. 5 (1): 48. дои:10.1186/s40168-017-0268-4. PMC 5410102. PMID 28454555.
- ^ а б Matamoros, Sebastien; Gras-Leguen, Christele; Le Vacon, Françoise; Potel, Gilles; de la Cochetiere, Marie-France (2013). "Development of intestinal microbiota in infants and its impact on health". Trends in Microbiology. 21 (4): 167–73. дои:10.1016/j.tim.2012.12.001. PMID 23332725.
- ^ а б c г. e f ж Mueller, Noel T.; Bakacs, Elizabeth; Combellick, Joan; Grigoryan, Zoya; Dominguez-Bello, Maria G. (2015). "The infant microbiome development: mom matters". Молекулалық медицинадағы тенденциялар. 21 (2): 109–17. дои:10.1016/j.molmed.2014.12.002. PMC 4464665. PMID 25578246.
- ^ Jiménez, Esther; Fernández, Leonides; Marín, María L; Martín, Rocío; Odriozola, Juan M; Nueno-Palop, Carmen; Narbad, Arjan; Olivares, Mónica; Xaus, Jordi; Rodríguez, Juan M (2005). "Isolation of Commensal Bacteria from Umbilical Cord Blood of Healthy Neonates Born by Cesarean Section". Қазіргі микробиология. 51 (4): 270–4. дои:10.1007/s00284-005-0020-3. PMID 16187156. S2CID 43438656.
- ^ Collado, Maria Carmen; Rautava, Samuli; Aakko, Juhani; Isolauri, Erika; Salminen, Seppo (2016). "Human gut colonisation may be initiated in utero by distinct microbial communities in the placenta and amniotic fluid". Ғылыми баяндамалар. 6: 23129. Бибкод:2016NatSR...623129C. дои:10.1038/srep23129. PMC 4802384. PMID 27001291.
- ^ Jiménez, Esther; Marín, María L.; Martín, Rocío; Odriozola, Juan M.; Olivares, Mónica; Xaus, Jordi; Fernández, Leonides; Rodríguez, Juan M. (2008). "Is meconium from healthy newborns actually sterile?". Микробиологиядағы зерттеулер. 159 (3): 187–93. дои:10.1016/j.resmic.2007.12.007. PMID 18281199.
- ^ Perez-Muñoz, Maria Elisa; Arrieta, Marie-Claire; Ramer-Tait, Amanda E; Walter, Jens (2017). "A critical assessment of the "sterile womb" and "in utero colonization" hypotheses: Implications for research on the pioneer infant microbiome". Микробиома. 5 (1): 48. дои:10.1186/s40168-017-0268-4. PMC 5410102. PMID 28454555.
- ^ Adlerberth, I; Wold, AE (2009). "Establishment of the gut microbiota in Western infants". Acta Paediatrica. 98 (2): 229–38. дои:10.1111/j.1651-2227.2008.01060.x. PMID 19143664. S2CID 205859933.
- ^ Coppa, G.V; Zampini, L; Galeazzi, T; Gabrielli, O (2006). "Prebiotics in human milk: A review". Ас қорыту және бауыр аурулары. 38: S291–4. дои:10.1016/S1590-8658(07)60013-9. PMID 17259094.
- ^ Fanaro, S; Chierici, R; Guerrini, P; Vigi, V (2007). "Intestinal microflora in early infancy: Composition and development". Acta Paediatrica. 92 (441): 48–55. дои:10.1111/j.1651-2227.2003.tb00646.x. PMID 14599042. S2CID 10316311.
- ^ Yassour, Moran; Vatanen, Tommi; Siljander, Heli; Hämäläinen, Anu-Maaria; Härkönen, Taina; Ryhänen, Samppa J; Franzosa, Eric A; Vlamakis, Hera; Хаттенхауэр, Кертис; Геверс, Дирк; Lander, Eric S; Knip, Mikael; Xavier, Ramnik J (2016). "Natural history of the infant gut microbiome and impact of antibiotic treatment on bacterial strain diversity and stability". Трансляциялық медицина. 8 (343): 343ra81. дои:10.1126/scitranslmed.aad0917. PMC 5032909. PMID 27306663.
- ^ а б c г. e f Ван, Ян; Kasper, Lloyd H (2014). "The role of microbiome in central nervous system disorders". Ми, мінез-құлық және иммунитет. 38: 1–12. дои:10.1016/j.bbi.2013.12.015. PMC 4062078. PMID 24370461.
- ^ а б Yoon, My Young; Lee, Keehoon; Yoon, Sang Sun (2014). "Protective role of gut commensal microbes against intestinal infections". Journal of Microbiology. 52 (12): 983–9. дои:10.1007/s12275-014-4655-2. PMID 25467115. S2CID 54622675.
- ^ Reinoso Webb, Cynthia; Koboziev, Iurii; Furr, Kathryn L; Grisham, Matthew B (2016). "Protective and pro-inflammatory roles of intestinal bacteria". Патофизиология. 23 (2): 67–80. дои:10.1016/j.pathophys.2016.02.002. PMC 4867289. PMID 26947707.
- ^ Mantis, N J; Rol, N; Corthésy, B (2011). "Secretory IgA's complex roles in immunity and mucosal homeostasis in the gut". Шырышты иммунология. 4 (6): 603–11. дои:10.1038/mi.2011.41. PMC 3774538. PMID 21975936.
- ^ а б Peterson, Lance W; Artis, David (2014). "Intestinal epithelial cells: Regulators of barrier function and immune homeostasis". Табиғатқа шолу Иммунология. 14 (3): 141–53. дои:10.1038/nri3608. PMID 24566914. S2CID 3351351.
- ^ а б Honda, Kenya; Littman, Dan R (2016). "The microbiota in adaptive immune homeostasis and disease". Табиғат. 535 (7610): 75–84. Бибкод:2016Natur.535...75H. дои:10.1038/nature18848. PMID 27383982. S2CID 4461492.
- ^ а б Levy, M.; Thaiss, C.A.; Elinav, E. (2016). "Metabolites: messengers between the microbiota and the immune system". Гендер және даму. 30 (14): 1589–97. дои:10.1101/gad.284091.116. PMC 4973288. PMID 27474437.
- ^ а б c г. e f ж сағ мен Zhang LS, Davies SS (April 2016). "Microbial metabolism of dietary components to bioactive metabolites: opportunities for new therapeutic interventions". Genome Med. 8 (1): 46. дои:10.1186/s13073-016-0296-x. PMC 4840492. PMID 27102537.
Лактобакиллус спп. convert tryptophan to indole-3-aldehyde (I3A) through unidentified enzymes [125]. Clostridium sporogenes convert tryptophan to IPA [6], likely via a tryptophan deaminase. ... IPA also potently scavenges hydroxyl radicals
Table 2: Microbial metabolites: their synthesis, mechanisms of action, and effects on health and disease
Figure 1: Molecular mechanisms of action of indole and its metabolites on host physiology and disease - ^ Wikoff WR, Anfora AT, Liu J, Schultz PG, Lesley SA, Peters EC, Сиуздак Г. (Наурыз 2009). "Metabolomics analysis reveals large effects of gut microflora on mammalian blood metabolites". Proc. Натл. Акад. Ғылыми. АҚШ. 106 (10): 3698–3703. дои:10.1073/pnas.0812874106. PMC 2656143. PMID 19234110.
Production of IPA was shown to be completely dependent on the presence of gut microflora and could be established by colonization with the bacterium Clostridium sporogenes.
IPA metabolism diagram - ^ "3-Indolepropionic acid". Human Metabolome Database. Альберта университеті. Алынған 12 маусым 2018.
Indole-3-propionate (IPA), a deamination product of tryptophan formed by symbiotic bacteria in the gastrointestinal tract of mammals and birds. 3-Indolepropionic acid has been shown to prevent oxidative stress and death of primary neurons and neuroblastoma cells exposed to the amyloid beta-protein in the form of amyloid fibrils, one of the most prominent neuropathologic features of Alzheimer's disease. 3-Indolepropionic acid also shows a strong level of neuroprotection in two other paradigms of oxidative stress. (PMID 10419516 ) ... More recently it has been found that higher indole-3-propionic acid levels in serum/plasma are associated with reduced likelihood of type 2 diabetes and with higher levels of consumption of fiber-rich foods (PMID 28397877 )
Origin: • Endogenous • Microbial - ^ Chyan YJ, Poeggeler B, Omar RA, Chain DG, Frangione B, Ghiso J, Pappolla MA (July 1999). "Potent neuroprotective properties against the Alzheimer beta-amyloid by an endogenous melatonin-related indole structure, indole-3-propionic acid". Дж.Биол. Хим. 274 (31): 21937–21942. дои:10.1074/jbc.274.31.21937. PMID 10419516.
[Indole-3-propionic acid (IPA)] has previously been identified in the plasma and cerebrospinal fluid of humans, but its functions are not known. ... In kinetic competition experiments using free radical-trapping agents, the capacity of IPA to scavenge hydroxyl radicals exceeded that of melatonin, an indoleamine considered to be the most potent naturally occurring scavenger of free radicals. In contrast with other antioxidants, IPA was not converted to reactive intermediates with pro-oxidant activity.
- ^ Rajilić-Stojanović, Mirjana; De Vos, Willem M (2014). "The first 1000 cultured species of the human gastrointestinal microbiota". FEMS микробиология шолулары. 38 (5): 996–1047. дои:10.1111/1574-6976.12075. PMC 4262072. PMID 24861948.
- ^ Hill, M. J. (March 1997). "Intestinal flora and endogenous vitamin synthesis". European journal of cancer prevention: the official journal of the European Cancer Prevention Organisation (ECP). 6 Suppl 1: S43–45. дои:10.1097/00008469-199703001-00009. ISSN 0959-8278. PMID 9167138.
- ^ "The Microbiome". Tufts Now. 2013-09-17. Алынған 2020-12-09.
- ^ а б c г. e ElRakaiby M, Dutilh BE, Rizkallah MR, Boleij A, Cole JN, Aziz RK (July 2014). "Pharmacomicrobiomics: the impact of human microbiome variations on systems pharmacology and personalized therapeutics". Омика. 18 (7): 402–414. дои:10.1089/omi.2014.0018. PMC 4086029. PMID 24785449.
The hundred trillion microbes and viruses residing in every human body, which outnumber human cells and contribute at least 100 times more genes than those encoded on the human genome (Ley et al., 2006), offer an immense accessory pool for inter-individual genetic variation that has been underestimated and largely unexplored (Savage, 1977; Medini et al., 2008; Minot et al., 2011; Wylie et al., 2012). ... Meanwhile, a wealth of literature has long been available about the biotransformation of xenobiotics, notably by gut bacteria (reviewed in Sousa et al., 2008; Rizkallah et al., 2010; Johnson et al., 2012; Haiser and Turnbaugh, 2013). This valuable information is predominantly about drug metabolism by unknown human-associated microbes; however, only a few cases of inter-individual microbiome variations have been documented [e.g., digoxin (Mathan et al., 1989) and acetaminophen (Clayton et al., 2009)].
- ^ а б c Cho I, Blaser MJ (March 2012). "The human microbiome: at the interface of health and disease". Табиғи шолулар. Генетика. 13 (4): 260–270. дои:10.1038/nrg3182. PMC 3418802. PMID 22411464.
The composition of the microbiome varies by anatomical site (Figure 1). The primary determinant of community composition is anatomical location: interpersonal variation is substantial23,24 and is higher than the temporal variability seen at most sites in a single individual25. ... How does the microbiome affect the pharmacology of medications? Can we “micro-type” people to improve pharmacokinetics and/or reduce toxicity? Can we manipulate the microbiome to improve pharmacokinetic stability?
- ^ Hutter T, Gimbert C, Bouchard F, Lapointe FJ (2015). "Being human is a gut feeling". Микробиома. 3: 9. дои:10.1186/s40168-015-0076-7. PMC 4359430. PMID 25774294.
Some metagenomic studies have suggested that less than 10% of the cells that comprise our bodies are Homo sapiens cells. The remaining 90% are bacterial cells. The description of this so-called human microbiome is of great interest and importance for several reasons. For one, it helps us redefine what a biological individual is. We suggest that a human individual is now best described as a super-individual in which a large number of different species (including Homo sapiens) coexist.
- ^ Kumar K, Dhoke GV, Sharma AK, Jaiswal SK, Sharma VK (January 2019). "Mechanistic elucidation of amphetamine metabolism by tyramine oxidase from human gut microbiota using molecular dynamics simulations". Жасушалық биохимия журналы. 120 (7): 11206–11215. дои:10.1002/jcb.28396. PMID 30701587. S2CID 73413138.
Particularly in the case of the human gut, which harbors a large diversity of bacterial species, the differences in microbial composition can significantly alter the metabolic activity in the gut lumen.4 Ішектің микробтық түрлерінің айырмашылығына байланысты дифференциалды метаболикалық белсенділік жақында метаболизмнің әртүрлі бұзылыстарымен және ауруларымен байланысты болды.5-12 Адамның әртүрлі ауруларындағы ішектің микробтық алуан түрлілігінің немесе дисбиоздың әсерінен басқа, ішек микробтарының әртүрлі ішілетін дәрілік молекулалардың биожетімділігі мен тиімділігіне ферментативті метаболизм арқылы әсер етуі мүмкін екендігін дәлелдейтін көптеген мәліметтер бар.13,14 ... Амфетаминнің тираминоксидазамен байланысуының және байланыстырылуының атомистикалық бөлшектері туралы осы зерттеу, осы ферменттің екі табиғи субстраттарымен, атап айтқанда, тирамин және фенилаланинмен салыстырумен, амфетаминнің тирамин оксидазасы арқылы метаболизмінің бұзылуына негізделген. E. coli ферменті. Алынған нәтижелер амфетаминнің суррогат молекуласын құрастыруда өте маңызды болады, ол бәсекеге қабілетті тежеу арқылы амфетамин препаратының тиімділігі мен биожетімділігін жақсартуға немесе дәрі-дәрмекті жақсы фармакологиялық әсер ету үшін қайта құруға көмектеседі. Бұл зерттеу сонымен қатар ішектің микробиотасын төмендетуге пайдалы клиникалық әсер етеді, бұл әртүрлі популяциялар арасында дәрілік реакцияның өзгеруіне әкеледі.
- ^ Соуса, Тиаго; Патерсон, Ронни; Мур, Ванесса; Карлссон, Андерс; Абрахамссон, Бертиль; Basit, Abdul W (2008). «Асқазан-ішек микробиотасы дәрілік заттардың биотрансформациясы алаңы ретінде». Халықаралық фармацевтика журналы. 363 (1–2): 1–25. дои:10.1016 / j.ijpharm.2008.07.009. PMID 18682282.
- ^ Хайзер, Х.Дж; Готенберг, Д.Б; Чатман, К; Сирасани, Г; Balskus, E. P; Тернбау, П.Ж (2013). «Адамның ішек бактериялары Eggerthella lenta арқылы жүрекке арналған дәрілерді инактивациялауды болжау және манипуляциялау». Ғылым. 341 (6143): 295–8. Бибкод:2013Sci ... 341..295H. дои:10.1126 / ғылым.1235872. PMC 3736355. PMID 23869020.
- ^ Майер, Э. А; Найт, Р; Мазманиан, С. К; Криан, Дж. Ф; Тиллиш, К (2014). «Ішек микробтары және ми: неврологиядағы парадигманың ауысуы». Неврология журналы. 34 (46): 15490–6. дои:10.1523 / JNEUROSCI.3299-14.2014. PMC 4228144. PMID 25392516.
- ^ а б c Динан, Тимоти Г; Криан, Джон Ф (2015). «Ішек микробиотасының миға және мінез-құлыққа әсері». Клиникалық тамақтану және метаболикалық күтім туралы қазіргі пікір. 18 (6): 552–8. дои:10.1097 / MCO.0000000000000221. PMID 26372511. S2CID 21424690.
- ^ а б c Карман, Роберт Дж .; Саймон, Мэри Элис; Фернандес, Хайде; Миллер, Маргарет А .; Бартоломей, Мэри Дж. (2004). «Ципрофлоксацин төмен деңгейде химиялық заттарда өсетін адамның нәжіс микрофлорасының колонизацияға төзімділігін бұзады». Нормативті токсикология және фармакология. 40 (3): 319–26. дои:10.1016 / j.yrtph.2004.08.005. PMID 15546686.
- ^ Брандт, Лоуренс Дж.; Бороди, Томас Юлиус; Кэмпбелл, Джордана (2011). «Эндоскопиялық фекальды микробиотаны трансплантациялау». Клиникалық гастроэнтерология журналы. 45 (8): 655–57. дои:10.1097 / MCG.0b013e3182257d4f. PMID 21716124.
- ^ Найт, DJW; Girling, KJ (2003). «Денсаулық пен аурудағы ішек флорасы». Лансет. 361 (9371): 512–19. дои:10.1016 / S0140-6736 (03) 13438-1. PMID 12781578. S2CID 40683723.
- ^ а б c Чо, Мен .; Яманиши, С .; Кокс, Л .; Мете, Б. А .; Завадил, Дж .; Ли, К .; Гао, З .; Махана, Д .; Раджу, К .; Тейтлер, I .; Ли, Х .; Алексеенко, А.В .; Blaser, J. J. (2012). «Антибиотиктер ерте өмір сүрген кезде ішек ішек микробиомы мен семіздікті өзгертеді». Табиғат. 488 (7413): 621–26. Бибкод:2012 ж. 488..621С. дои:10.1038 / табиғат11400. PMC 3553221. PMID 22914093.
- ^ а б c г. Шнайдерхан, Дж; Мастер-Аңшы, Т; Локк, А (2016). «Ауруды емдеу және алдын-алу үшін ішек флорасын мақсаттандыру». Отбасылық тәжірибе журналы. 65 (1): 34–8. PMID 26845162.
- ^ Бейкер, Моня (2012). «Жүктілік ішек ішек микробтарын өзгертеді». Табиғат. дои:10.1038 / табиғат.2012.11118. S2CID 87078157.
- ^ Хилл, Колин; Гуарнер, Франциско; Рейд, Грегор; Гибсон, Гленн Р. Меренштейн, Даниэл Дж; Пот, Бруно; Морелли, Лоренцо; Канани, Роберто Берни; Флинт, Гарри Дж; Сальминен, Сеппо; Кальдер, Филипп С; Сандерс, Мэри Эллен (2014). «Пробиотиктер мен пребиотиктердің халықаралық ғылыми ассоциациясы пробиотик терминін қолдану аясы мен қолдану туралы консенсус тұжырымы». Табиғи шолулар Гастроэнтерология және гепатология. 11 (8): 506–14. дои:10.1038 / nrgastro.2014.66. PMID 24912386.
- ^ Райкерс, Гер Т; Де Вос, Виллем М; Бруммер, Роберт-Ян; Морелли, Лоренцо; Кортье, Жерар; Марто, Филипп (2011). «Пробиотиктердің денсаулыққа пайдасы және денсаулыққа қатысты талаптар: ғылым мен маркетингті кеңейту». Британдық тамақтану журналы. 106 (9): 1291–6. дои:10.1017 / S000711451100287X. PMID 21861940.
- ^ Хэткинс, Роберт В. Крумбек, Жанина А; Bindels, Laure B; Кани, Патрис Д; Фахей, Джордж; Гох, Ён Джун; Хэмакер, Брюс; Мартенс, Эрик С; Миллс, Дэвид А; Расталь, Роберт А; Вон, Элейн; Сандерс, Мэри Эллен (2016). «Пребиотиктер: анықтамалар неге маңызды». Биотехнологиядағы қазіргі пікір. 37: 1–7. дои:10.1016 / j.copbio.2015.09.001. PMC 4744122. PMID 26431716.
- ^ Панди, Кавита. R; Наик, Суреш. R; Вакил, Бабу. V (2015). «Пробиотиктер, пребиотиктер және синбиотиктер - шолу». Азық-түлік ғылымдары және технологиялар журналы. 52 (12): 7577–87. дои:10.1007 / s13197-015-1921-1. PMC 4648921. PMID 26604335.
- ^ Бруккс, Жералдин; Ванденхувель, Дитер; Клес, Ингмар Дж. Дж .; Лебир, Сара; Киекенс, Филипп (2016). «Пробиотикалық бактерияларды кептіру әдістері жаңа фармакотиктерді дамытуға маңызды қадам ретінде». Халықаралық фармацевтика журналы. 505 (1–2): 303–18. дои:10.1016 / j.ijpharm.2016.04.002. hdl:10067/1328840151162165141. PMID 27050865.
- ^ Sleator, Roy D; Хилл, Колин (2009). «Жақсартылған фарбиотиктердің ұтымды дизайны». Биомедицина және биотехнология журналы. 2009: 275287. дои:10.1155/2009/275287. PMC 2742647. PMID 19753318.
- ^ Паттерсон, Элейн; Криан, Джон Ф; Фицджералд, Джералд Ф; Росс, Р.Пол; Динан, Тимоти Г; Стэнтон, Кэтрин (2014). «Ішек микробиотасы, олар шығаратын және денсаулықты қамтамасыз ететін фарбиотиктер». Тамақтану қоғамының еңбектері. 73 (4): 477–89. дои:10.1017 / S0029665114001426. PMID 25196939.
- ^ Форд, Александр С; Квигли, Эамонн М М; Лэйси, Брайан Е; Лембо, Энтони Дж; Сайто, Юрий А; Шиллер, Лоуренс Р; Соффер, Эди Е; Шпигель, Бреннан М Р; Moayyedi, Paul (2014). «Тітіркенетін ішек синдромындағы пребиотиктер, пробиотиктер және синбиотиктер тиімділігі және созылмалы идиопатиялық іш қату: жүйелік шолу және мета-анализ». Американдық гастроэнтерология журналы. 109 (10): 1547-61, викторина 1546, 1562. дои:10.1038 / ajg.2014.202 ж. PMID 25070051. S2CID 205100508.
- ^ Дюпон, Эндрю; Ричардс; Джелинек, Кэтрин А; Крилл, Джозеф; Рахими, Эрик; Гурури, Йезаз (2014). «Ішектің қабыну ауруы кезіндегі пробиотиктердің, пребиотиктердің және синбиотиктердің рандомизацияланған бақыланатын зерттеулеріне жүйелік шолу». Клиникалық және эксперименттік гастроэнтерология. 7: 473–87. дои:10.2147 / CEG.S27530. PMC 4266241. PMID 25525379.
- ^ Ю, Ченг Гонг; Хуанг, Цинь (2013). «Ішектің микробиотасының ішектің қабыну ауруының патогенезіндегі рөлі туралы соңғы прогресс». Асқорыту аурулары журналы. 14 (10): 513–7. дои:10.1111/1751-2980.12087. PMID 23848393. S2CID 26982085.
- ^ Майер, Лиза; Прутеану, Михаела; Кун, Майкл; Целлер, Георг; Тельцеров, Анья; Андерсон, Экзен Эрин; Брочадо, Ана Рита; Фернандес, Кит Конрад; Доза, Хитоми; Мори, Хиротада; Патил, Киран Раосахеб; Борк, тең; Typas, Athanasios (2018). «Антибиотик емес дәрілердің адамның ішек бактерияларына кең әсер етуі». Табиғат. 555 (7698): 623–628. Бибкод:2018 ж. Табиғат 555..623М. дои:10.1038 / табиғат 25979. PMC 6108420. PMID 29555994.
- ^ а б Камбодж, АК; Коттер, ТГ; Оксентенко, А.С. (2017). «Хеликобактерия: менеджменттің өткені, бүгіні және болашағы». Mayo клиникасының материалдары. 92 (4): 599–604. дои:10.1016 / j.mayocp.2016.11.017. ISSN 0025-6196. PMID 28209367.
- ^ а б c «Ойық жара ауруы» (PDF). Джонс Хопкинс университетінің медицина мектебі. 2013 жыл. Алынған 21 қазан 2020.
- ^ Буриш, Йохан; Джесс, Тайн; Мартинато, Маттео; Лакатос, Питер Л (2013). «Еуропадағы ішектің қабыну ауруы». Крон және колит журналы. 7 (4): 322–37. дои:10.1016 / j.crohns.2013.01.010. PMID 23395397.
- ^ Бландино, Дж; Интурри, Р; Лаззара, Ф; Ди Роза, М; Малагуарнера, Л (2016). «Ішек микробиотасының қант диабетіне әсері». Қант диабеті және метаболизм. 42 (5): 303–315. дои:10.1016 / j.diabet.2016.04.004. PMID 27179626.
- ^ а б c Буланже, Клэр Л; Невес, Ана Луиза; Шилло, Джульен; Николсон, Джереми К; Дюма, Марк-Эммануэль (2016). «Ішек микробиотасының қабынуға, семіздікке және метаболизм ауруларына әсері». Геномдық медицина. 8 (1): 42. дои:10.1186 / s13073-016-0303-2. PMC 4839080. PMID 27098727.
- ^ Спиллер, Робин (2016). «Ішектің тітіркену синдромы: симптомдардың пайда болу механизмдері туралы жаңа түсініктер және емдеудегі жетістіктер». F1000Зерттеу. 5: 780. дои:10.12688 / f1000 іздеу.7992.1. PMC 4856111. PMID 27158477.
- ^ а б c Арриета, Мари-Клер; Стимсма, Лия Т; Димитриу, Педро А; Торсон, Лиза; Рассел, Шеннон; Юрист-Доутч, Софи; Кузельевич, Борис; Алтын, Мэттью Дж; Бриттон, Хайди М; Лефевр, Диана Л; Суббаро, Падмажа; Мандхан, Пиуш; Беккер, Аллан; Макнагни, Келли М; Sears, Malcolm R; Коллманн, Тобиас; Мох, Уильям В. Турви, Стюарт Е; Бретт Финлей, Б (2015). «Ерте нәресте кезіндегі микробтық және метаболикалық өзгерістер балалық демікпе қаупіне әсер етеді». Трансляциялық медицина. 7 (307): 307ra152. дои:10.1126 / scitranslmed.aab2271. PMID 26424567. S2CID 206687974.
- ^ а б Стимсма, Лия Т; Турви, Стюарт Е (2017). «Демікпе және микробиома: өмірдің маңызды кезеңін анықтау». Аллергия, астма және клиникалық иммунология. 13: 3. дои:10.1186 / s13223-016-0173-6. PMC 5217603. PMID 28077947.
- ^ Ипчи, Қаған; Алтынтопрак, Ниязи; Мулук, Нурай Баяр; Сентюрк, Мехмет; Цинги, Джемал (2016). «Аллергиялық аурулар кезіндегі адам микробиомының мүмкін механизмдері». Еуропалық Ото-Рино-Ларингология мұрағаты. 274 (2): 617–626. дои:10.1007 / s00405-016-4058-6. PMID 27115907. S2CID 27328940.
- ^ Марино, Э., Ричардс, Дж.Л., Маклеод, Х., Стэнли, Д., Яп, Я.А., Найт, Дж., Маккензи, С., Кранич, Дж., Оливейра, AC, Росселло, Ф.Ж., Кришнамурти, Б., Nefzger, CM, Macia, L., Thorburn, A., Baxter, AG, Morahan, G., Wong, LH, Polo, JM, Moore, RJ,… Mackay, CR (2017). Ішектің микробтық метаболиттері аутоиммунды Т жасушаларының жиілігін шектейді және 1 типті қант диабетінен қорғайды. Табиғат иммунологиясы, 18 (5), 552-562. https://doi.org/10.1038/ni.3713
- ^ Bettelli E, Carrier Y, Gao W, Korn T, Strom TB, Oukka M, Weiner HL, Kuchroo VK (мамыр 2006). «TH17 патогенді эффектор мен генераторлық Т-жасушалар генерациясының өзара даму жолдары». Табиғат. 441 (7090): 235–8. Бибкод: 2006 ж.441..235B. дои: 10.1038 / nature04753. PMID 16648838.
- ^ а б SÄEMANN, M. D., BÖHMIG, G. A., ÖSTERREICHER, C. H., BURTSCHER, H., PAROLINI, O., DIAKOS, C., STÖCKL, J., HÖRL, W. H., & ZLABINGER, G. J. (2000). Натрий бутиратының адам моноциттеріне қабынуға қарсы әсері: ИЛ-12-нің күшті тежелуі және ИЛ-10 өндірісінің реттелуі. FASEB журналы, 14 (15), 2380–2382. https://doi.org/10.1096/fj.00-0359fje
- ^ Гао, Z; Ин, Дж; Чжан, Дж; Уорд, Р. Мартин, Дж .; Лефевре, М; Цефалу, В. Ye, J (2009). «Бутырат инсулинге сезімталдықты жақсартады және тышқандардағы энергия шығынын арттырады». Қант диабеті. 58 (7): 1509–17. дои:10.2337 / db08-1637. PMC 2699871. PMID 19366864.
- ^ Мазиди, Мохсен; Резаи, Пейман; Кенге, Андре Паскаль; Мобархан, Маджид Гаюр; Папоротниктер, Гордон А (2016). «Ішек микробиомасы және метаболикалық синдром». Қант диабеті және метаболикалық синдром: клиникалық зерттеулер және шолулар. 10 (2): S150-7. дои:10.1016 / j.dsx.2016.01.024. PMID 26916014.
- ^ Чен, Сяо; д'Суза, Рошан; Hong, Seong-Tshool (2013). «Ішек-ми осіндегі ішек микробиотасының рөлі: қазіргі қиындықтар мен перспективалар». Ақуыз және жасуша. 4 (6): 403–14. дои:10.1007 / s13238-013-3017-x. PMC 4875553. PMID 23686721.
- ^ а б Минемура, Масами (2015). «Ішек микробиотасы және бауыр аурулары». Дүниежүзілік гастроэнтерология журналы. 21 (6): 1691–702. дои:10.3748 / wjg.v21.i6.1691. PMC 4323444. PMID 25684933.
- ^ Син, Николас Л; Тенг, Мишель W L; Мок, Тони С К; Soo, Ross A (2017). «Де-ново және иммундық бақылау-өткізу пунктіне бағытталған қарсылық». Лансет онкологиясы. 18 (12): e731-41. дои:10.1016 / s1470-2045 (17) 30607-1. PMID 29208439.
- ^ а б Меллер, Эндрю Х .; Ли, Инингин; Ngole, Eitel Mpoudi; Ахука-Мундеке, Стив; Лонсдорф, Элизабет V .; Пуси, Энн Е .; Питерс, Мартин; Хан, Беатрис Х .; Охман, Ховард (2014-11-18). «Адам эволюциясы кезінде ішектің микробиомасындағы жылдам өзгерістер». Ұлттық ғылым академиясының материалдары. 111 (46): 16431–16435. Бибкод:2014 PNAS..11116431M. дои:10.1073 / pnas.1419136111. ISSN 0027-8424. PMC 4246287. PMID 25368157.
- ^ Энгель, П .; Моран, Н. (2013). «Жәндіктердің ішек микробиотасы - құрылымы мен қызметіндегі әртүрлілік». FEMS микробиология шолулары. 37 (5): 699–735. дои:10.1111/1574-6976.12025. PMID 23692388.
- ^ Brune, A. (2014). «Терминит ішектерінде лигноцеллюлозаның симбиотикалық қорытылуы». Микробиологияның табиғаты туралы шолулар. 12 (3): 168–80. дои:10.1038 / nrmicro3182. PMID 24487819. S2CID 5220210.
- ^ а б Дитрих, С .; Кёлер, Т .; Brune, A. (2014). «Термит ішек микробиотасының тарақанының шығу тегі: бактериялық қауымдастық құрылымындағы заңдылықтар негізгі эволюциялық оқиғаларды көрсетеді». Қолданбалы және қоршаған орта микробиологиясы. 80 (7): 2261–69. дои:10.1128 / AEM.04206-13. PMC 3993134. PMID 24487532.
- ^ а б Микаелян, А .; Дитрих, С .; Кёлер, Т .; Пулсен, М .; Силлам-Дюсс, Д .; Brune, A. (2015). «Диета - жоғары термиттердің ішектеріндегі бактериялық қауымдастық құрылымының негізгі анықтаушысы». Молекулалық экология. 24 (20): 5824–95. дои:10.1111 / mec.13376. PMID 26348261. S2CID 206182668.
- ^ Микаелян, А .; Томпсон, С .; Хофер, М .; Brune, A. (2016). «Микробсыз тарақан ішектеріндегі күрделі бактериалды бірлестіктердің детерминирленген жиынтығы». Қолданбалы және қоршаған орта микробиологиясы. 82 (4): 1256–63. дои:10.1128 / AEM.03700-15. PMC 4751828. PMID 26655763.
Әрі қарай оқу
- Мақалаларға шолу жасаңыз
- Марандуба, Карлос Магно да Коста; Де Кастро, Сандра Бертелли Рибейро; Соуза, Густаво Торрес де; Россато, Криштиану; Да Гуиа, Франциско Карлос; Валенте, Мария Анете Сантана; Ретторе, Джоа Витор Пейс; Марандуба, Клаудинея Перейра; Соуза, Камила Маурман де; Кармо, Антонио Марсио Ресенде жасайды; MacEdo, Джилсон Коста; Силва, Фернандо де Са (2015). «Иммундық жүйенің және нейроиммундық жүйенің модуляторы ретіндегі ішек микробиотасы: иенің денсаулығы мен гомеостазға әсері». Иммунологияны зерттеу журналы. 2015: 931574. дои:10.1155/2015/931574. PMC 4352473. PMID 25759850.
- Де Претер, Викки; Хамер, Хенрике М; Уинди, Карен; Вербеке, Кристин (2011). «Алдын-ала және / немесе пробиотиктердің адамның ішектің метаболизміне әсері: бұл адамның денсаулығына әсер ете ме?». Молекулалық тамақтану және тағамды зерттеу. 55 (1): 46–57. дои:10.1002 / mnfr.201000451. PMID 21207512.
- Пракаш, Сатя; Родез, Лаетия; Коуса-Чарли, Майкл; Томаро-Дюшно, Кэтрин; Томаро-Дюческо, Кэтрин; Коуса-Чарли; Rodes (2011). «Ішек микробиотасы: адам денсаулығы мен биотерапевтика дамуын түсінудің келесі шегі». Биологиялық заттар: мақсаттар және терапия. 5: 71–86. дои:10.2147 / BTT.S19099. PMC 3156250. PMID 21847343.
- Ву, Г.Д .; Чен Дж .; Гофман, С .; Биттингер, К .; Чен, Y.-Y .; Килбауг, С.А .; Бевтра, М .; Найтс, Д .; Уолтерс, В.А .; Найт, Р .; Синха, Р .; Гилрой, Э .; Гупта, К .; Балдасано, Р .; Нессель, Л .; Ли, Х .; Бушман, Ф. Д .; Льюис, ДжД (2011). «Ұзақ мерзімді диеталық қалыптарды ішектің микробтық энтеротиптерімен байланыстыру». Ғылым. 334 (6052): 105–08. Бибкод:2011Sci ... 334..105W. дои:10.1126 / ғылым.1208344. PMC 3368382. PMID 21885731.

