Комбинаторлық химия - Википедия - Combinatorial chemistry
Комбинаторлық химия тұрады химиялық синтетикалық әдістер бұл бір процесте көптеген қосылыстарды (оннан мыңға, тіпті миллионға дейін) дайындауға мүмкіндік береді. Мыналар құрама кітапханалар қоспалар, жеке қосылыстар жиынтығы немесе компьютерлік бағдарламалық жасақтамадан туындайтын химиялық құрылымдар түрінде жасалуы мүмкін.[1] Комбинаторлық химия ұсақ молекулалардың синтезі үшін және пептидтер үшін қолданыла алады.
Кітапханалардың пайдалы компоненттерін анықтауға мүмкіндік беретін стратегиялар комбинаториялық химияның бөлігі болып табылады. Комбинаторлық химияда қолданылатын әдістер химиядан тыс қолданылады.
Тарих
Комбинаторлық химияны 1982 жылы нотариалды куәландырылған құжатта оның принципін, комбинаторлық синтезді және деконволюция процедурасын сипаттаған Фурка Á (Этвош Лоранд университеті Будапешт Венгрия) ойлап тапқан.[2] Комбинаторлық әдістің принципі: көп компонентті қоспа қоспасын (комбинаториялық кітапхана) бір сатылы процедурада синтездеу және есірткіге немесе басқа пайдалы қосылыстардың басқа түрлерін бір процесте табу үшін оны скринингтен өткізу. Комбинаторлық әдістің ең маңызды жаңалығы - синтездеу мен скринингте процестің жоғары өнімділігін қамтамасыз ететін қоспаларды қолдану. Өнертабысқа себеп болған уәждемелер 2002 жылы жарияланған болатын.[3]
Кіріспе
А молекулаларының синтезі комбинаторлық сән молекулалардың көп мөлшеріне тез әкелуі мүмкін. Мысалы, әртүрліліктің үш нүктесі бар молекула (R1, R2, және R3) генерациялай алады мүмкін құрылымдар, қайда , , және әр түрлі алмастырғыштардың нөмірлері.[2]
Комбинаторлық химияның негізгі принципі - дайындау кітапханалар қосылыстардың өте көп мөлшері, содан кейін кітапханалардың пайдалы компоненттерін анықтайды.
Комбинаторлық химияны өнеркәсіп 90-шы жылдардан бастап шынымен қолға алғанымен,[4] оның тамыры сонау 1960 жылдары зерттеуші болған кезде байқалады Рокфеллер университеті, Брюс Меррифилд, тергеуді бастады қатты фазалық синтез туралы пептидтер.
Комбинаторлық химия өзінің қазіргі заманғы формасында ең үлкен әсер еткен шығар фармацевтикалық өнеркәсіп.[5] Зерттеушілер қосылыс белсенділігі профилін оңтайландыруға тырысадыкітапхана 'әр түрлі, бірақ байланысты қосылыстардан тұрады.[дәйексөз қажет ] Аванстар робототехника компанияларға жылына 100000-нан астам жаңа және бірегей қосылыстар шығаруға мүмкіндік беретін комбинаторлық синтездің өндірістік тәсілін әкелді.[6]
Көптеген құрылымдық мүмкіндіктерді басқару үшін зерттеушілер «виртуалды кітапхана» құрады, берілген құрылымның барлық мүмкін құрылымдарын есептеу фармакофор барлығымен реактивтер.[7] Мұндай кітапхана мыңнан миллионға дейінгі «виртуалды» қосылыстардан тұруы мүмкін. Зерттеуші әр түрлі есептеулер мен критерийлерге сүйене отырып, нақты синтез үшін «виртуалды кітапхананың» ішкі жиынын таңдайды (қараңыз) ADME, есептеу химиясы, және QSAR ).
Полимерлер (пептидтер мен олигонуклеотидтер)
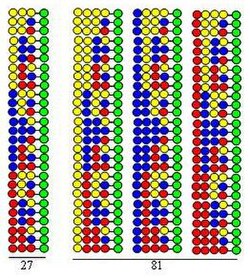
Комбинаторлық сплит-микс (сплит және бассейн) синтезі
Комбинаторлық сплит-микс (сплит және бассейн) синтезі [8] [9] негізделеді қатты фазалық синтез әзірлеген Merrifield.[10] Егер комбинаториялық пептидтік кітапхана 20 көмегімен синтезделсе аминқышқылдары (немесе құрылыс блоктарының басқа түрлері) қатты тіреуішті құрайтын моншақ 20 тең бөлікке бөлінеді. Осыдан кейін әр бөлікке әр түрлі амин қышқылын қосады. Үшінші қадам - барлық бөліктерді араластыру. Осы үш қадам циклды қамтиды. Пептидтік тізбектердің созылуын цикл қадамдарын қайталау арқылы жүзеге асыруға болады.

Процедура а синтезімен көрсетілген дипептид екі циклдегі құрылыс блоктары сияқты бірдей үш аминқышқылын қолданатын кітапхана. Бұл кітапхананың әр компонентінде әр түрлі тәртіпте орналасқан екі амин қышқылы бар. Муфталарда қолданылатын амин қышқылдары суреттегі сары, көк және қызыл шеңберлермен көрсетілген. Дивергентті көрсеткілер қатты тіреуіш шайырды (жасыл шеңберлерді) тең бөліктерге бөлуді көрсетеді, тік көрсеткілер ілінісуді білдіреді және конвергентті көрсеткілер тірек бөліктерін араластырып, біртектес етеді.
Суретте екі синтетикалық циклда 9 дипептид түзілетіні көрсетілген. Үшінші және төртінші циклдарда сәйкесінше 27 трипептид және 81 тетрапептид түзіледі.
«Сплит-микс синтезінің» бірнеше тамаша ерекшеліктері бар:
- Бұл өте тиімді. Суретте көрсетілгендей, синтетикалық процесте түзілген пептидтер саны (3, 9, 27, 81) орындалған циклдар санымен экспоненциалды түрде артады. Әрбір синтетикалық циклде 20 амин қышқылын қолдану арқылы түзілген пептидтердің саны: сәйкесінше 400, 8000, 160000 және 3.200.000. Бұл пептидтер саны орындалған циклдар санымен экспоненциалды түрде көбейетіндігін білдіреді.
- Барлық пептидтік тізбектер процесте пайда болады, оларды циклдарда қолданылатын аминқышқылдарының тіркесімі арқылы шығаруға болады.
- Қолдауды тең үлгілерге бөлу кітапхана компоненттерінің тең молярлық мөлшерде қалыптасуын қамтамасыз етеді.
- Тіректің әр моншағында тек жалғыз пептид пайда болады. Ілінісу сатысында тек бір аминқышқылын қолдану салдары. Таңдалған бисерді алатын пептидтің қандай екендігі мүлдем белгісіз.
- Сплит-микс әдісі органикалық немесе кез-келген басқа типтегі кітапхананы синтездеу үшін пайдаланылуы мүмкін, оны сатылы процесте оның блоктарынан жасауға болады.
1990 жылы үш топ пептидтік кітапханаларды биологиялық әдістермен дайындау әдістерін сипаттады[11][12][13] және бір жылдан кейін Фодор және басқалар. ұсақ шыны слайдтарда пептидтік массивтерді синтездеудің керемет әдісін жариялады.[14]
Марио Гейсен және оның әріптестері пептидтік массивтерді дайындау үшін «параллель синтез» әдісін жасады.[15] Олар 96 пептидтерді қатты тірекпен ұштарында қапталған пластик таяқшаларға (түйреуіштерге) синтездеді. Штырлар а ұңғымаларына орналастырылған реактивтердің ерітіндісіне батырылды микротрит тәрелке. Әдіс автоматты параллельді синтезаторларды қолдану арқылы кеңінен қолданылады. Параллель әдіс нақты комбинаторлыққа қарағанда әлдеқайда баяу болғанымен, оның артықшылығы - әр түйреуіште қандай пептидтің немесе басқа қосылыстың пайда болатындығы дәл белгілі.
Сплит-микстің де, параллель синтездің де артықшылықтарын біріктіретін әрі қарайғы процедуралар жасалды. Екі топ сипаттаған әдіс бойынша[16][17] қатты тіреуіш капсулада түзілетін қосылыстың кодын тасымалдайтын радиожиілік белгісімен бірге өткізгіш пластикалық капсулаларға салынған. Процедура сплит-микс әдісіне ұқсас жүргізілді. Бөлінген сатыда капсулалар реакциялық ыдыстар арасында капсулалардың радиожиілік белгілерінен оқылған кодтарға сәйкес бөлінді.
Сол мақсаттағы басқа әдісті Фурка және басқалар жасады.[18] «жол синтезі» деп аталады. Бұл әдіспен капсулаларда ешқандай код жоқ. Олар алқадағы інжу-маржандай тізіліп, жіп түрінде реакция ыдыстарына орналастырылады. Капсулалардың сәйкестігі, сондай-ақ олардың құрамы жіптерде орналасқан күйімен сақталады. Әрбір ілінісу қадамынан кейін капсулалар белгілі бір ережелерге сәйкес жаңа жолдар арасында қайта бөлінеді.
Шағын молекулалар
Бұл бөлім сияқты оқылады шолу тақырыптың энциклопедиялық сипаттамасынан гөрі. (Шілде 2018) |
Дәрілерді табу процесінде синтез және биологиялық бағалау шағын молекулалар қызығушылық, әдетте, ұзақ және ауыр жұмыс болды. Комбинаторлық химия соңғы онжылдықтарда дәрі-дәрмектің кішігірім молекулаларына үміткерлердің көп мөлшерін тез және тиімді синтездеу тәсілі ретінде пайда болды. Әдеттегі синтезде синтетикалық схеманың соңында тек бір мақсатты молекула жасалады, синтездегі әр сатыда тек бір өнім шығады. Ішінде комбинаторлық синтез, тек бір бастапқы затты қолданғанда молекулалардың үлкен кітапханасын бірдей реакция жағдайларын пайдаланып синтездеуге болады, содан кейін оларды тексеруге болады биологиялық белсенділік. Содан кейін бұл өнімдер пулы үш өнімнің әрқайсысы бар үш тең бөлікке бөлінеді, содан кейін үш жеке бассейннің әрқайсысы басқа B, C немесе D реагент бірлігімен реакцияға түсіп, алдыңғы 3-тен 9 бірегей қосылыстар шығарады. Содан кейін бұл процесс көптеген қосылыстар тудыратын құрылыс материалдарының қажетті саны қосылғанға дейін қайталанады. Қосылыстар кітапханасын көп сатылы синтездеу арқылы синтездеу кезінде реакцияның тиімді әдістерін қолдану қажет, егер әр реакция сатысынан кейін дәстүрлі тазарту әдістері қолданылса, өнімділік пен тиімділікке зиян келеді.
Қатты фазалық синтез синтетикалық химияда жиі қолданылатын типтік сөндіру және тазарту сатыларының қажеттілігін жою үшін әлеуетті шешімдер ұсынады. Жалпы алғанда, бастапқы молекула қатты тірекке жабысады (әдетте an ерімейтін полимер ), содан кейін қосымша реакциялар жүргізіліп, соңғы өнім тазартылады, содан кейін қатты тіректен бөлінеді. Қызығушылық молекулалары қатты тірекке бекітілгендіктен, синтетикалық химияға ең көп қажет ететін сұйық-сұйықтық экстракциясы мен еріткіштің булану сатыларының қажеттілігін жоққа шығарып, әрбір реакциядан кейін бір сүзу / жуу сатысына дейін тазартуды азайтуға болады. Сонымен қатар, гетерогенді реактивтерді қолдану арқылы артық реактивтерді аяқтауға дейінгі баяу реакцияларды қозғау үшін қолдануға болады, бұл өнімділікті одан әрі жақсартуға мүмкіндік береді. Артық реагенттерді тазалаудың қосымша сатыларын қажет етпей жай ғана жууға болады хроматография.

Осы жылдары қатты фазалы органикалық синтезді комбинаторлық химияда қолдануды нақтылаудың әр түрлі әдістері, соның ішінде синтездеу мен тазартудың қарапайымдылығын арттыруға бағытталған күштер, сонымен қатар аралық өнімдерді сипаттайтын дәстүрлі емес әдістер жасалды. Мұнда сипатталған мысалдардың көпшілігінде реакцияның әр сатысында гетерогенді реакция ортасы қолданылады, Бут пен Ходжес қатты дәнекерлі реактивтерді дәстүрлі ерітінді-фазалық синтездерді тазарту сатысында ғана қолданудың алғашқы үлгісін ұсынады.[19] Олардың ойынша, ерітінді фазалық химия молекулаларды шайырларға бекіту және алу үшін қажет болатын қосылу мен бөлшектеу реакцияларынан аулақ болудың, сондай-ақ белгіленген фазалық реакциялардың қатты фазалық аналогтарын қайта құру қажеттілігін болдырмайтын артықшылықтарды ұсынады.
Синтездің соңындағы жалғыз тазарту сатысы бұзылған қоспаның химиялық құрылымы белгілі болған жағдайда бір немесе бірнеше қоспаларды кетіруге мүмкіндік береді. Қатты тірек реагенттерді қолдану қосылыстардың синтезін едәуір жеңілдетсе, көптеген комбинаторлық синтездер бірнеше сатыларды қажет етеді, олардың әрқайсысы әлі де тазартудың қандай да бір түрін қажет етеді. Армстронг және т.б. көп компонентті конденсациялар (МКК) деп аталатын комбинаторлық кітапханаларды құрудың бір кәстрөлді әдісін сипаттаңыз.[20] Бұл схемада үш немесе одан да көп реагенттер реакция жасайды, сондықтан әрбір реагент соңғы өнімге бір сатыда енгізіліп, көптеген тазарту кезеңдерін қамтитын көп сатылы синтездің қажеттілігі алынып тасталады. MCC-де қандай қосылыстардың биологиялық-белсенді екенін анықтау үшін деконволюция қажет емес, өйткені массивтегі әрбір синтезде тек бір ғана өнім болады, сондықтан қосылыстың сәйкестігі сөзсіз белгілі болуы керек.
Басқа массив синтезінде әлі де үлкен кітапхана құрылды олигопептидтер сплит синтезі арқылы.[21] Көптеген мың қосылыстар жасаудың жетіспеушілігі - түзілген қосылыстардың құрылымын анықтау қиын. Олардың шешімі молекулярлық тегтерді қолдану болып табылады, мұнда бисерге аз мөлшерде (1 пмоль / моншақ) бояғыш қосылады және белгілі бір моншақтың сәйкестігін моншақта қандай тегтер бар екенін анықтауға болады. Тегтерді бекіту рецепторларды сәйкестендіруді қаншалықты жеңілдететініне қарамастан, әр қосылысты рецепторлардың байланыстыру қабілеті үшін жеке скринингтен өткізу мүмкін емес болар еді, сондықтан әр рецепторға бояғыш қосылды, тек олардың субстратымен байланысатын рецепторлар ғана түс өзгеруін тудырады.
Массивте көптеген реакцияларды жүргізу қажет болғанда (мысалы, Армстронгтың MCC массивтерінің бірінде сипатталған 96 реакция), тиімділікті жақсарту үшін синтездің кейбір жалықтыратын аспектілерін автоматтандыруға болады. DeWitt және Czarnik «деп аталатын әдісті егжей-тегжейлі сипаттайды.DIVERSOMER әдісі, «онда көптеген химиялық реакциялардың миниатюраланған нұсқалары бір уақытта жүреді.[22] Бұл әдіс шайырды тиеу және жуу циклдарын, сондай-ақ реакция циклін бақылауды және тазартуды автоматтандыратын құрылғыны пайдаланады және олардың әдісі мен аппараттарының орындылығын көрсетеді, мысалы, әртүрлі молекулалар кластарын синтездеу үшін. гидантоиндер және бензодиазепиндер, көп жағдайда 40 жеке реакцияны жүргізу.
Көбінесе қымбат жабдықты пайдалану мүмкін емес, және Швабахер және т.б. кітапхана мүшелерінің параллель синтезін және қосылыстардың бүкіл кітапханаларын бағалауды біріктірудің қарапайым әдісін сипаттаңыз.[23] Олардың әдісінде әр түрлі аймақтарға бөлінген жіп цилиндрге оралады, содан кейін әр түрлі реактив тек бір түрге ие әр аймаққа қосылады. Содан кейін жіп қайтадан бөлініп, басқа өлшемдегі цилиндрге оралады, содан кейін бұл процесс қайталанады. Бұл әдістің әсемдігі мынада: әр өнімнің сәйкестігін оның жіп бойымен орналасуы арқылы білуге болады, ал сәйкес биологиялық белсенділік Флуоресценция сигналдарының Фурье түрлендіруі.
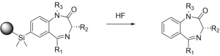
Мұнда сипатталған синтездердің көпшілігінде бастапқы реагентті қатты тірекке қосу / алып тастау қажет. Бұл гидроксил тобының пайда болуына әкелуі мүмкін, бұл мақсатты қосылыстың биологиялық белсенділігіне әсер етуі мүмкін. Эллман көп сатылы синтез схемасында қатты фазалық тіректерді пайдаланады, олар белгілі терапевтік агенттер болып табылатын 192 жеке 1,4-бензодиазепин туындыларын алады.[24] Потенциалды гидроксилді топ интерференциясының мүмкіндігін болдырмау үшін, силил-арил химиясын қолдана отырып, молекулаларды тіректен бөлінетін және байланыстырушы із қалдырмайтын қатты тірекке байланыстыратын жаңа әдіс қолданылады.

Молекуланы қатты тірекке бекіту кезінде молекуланы шайырдан бөлмей, аралық заттарды бір-бірінен оқшаулауға болмайды. Реакцияның ілгерілеуін бақылау және өнімнің құрылымын растау үшін қолданылатын дәстүрлі сипаттамалардың көптеген әдістері шешімге негізделген болғандықтан, әртүрлі әдістер қолданылуы керек. Гель-фаза 13 С NMR спектроскопиясы, MALDI масс-спектрометриясы және IR спектроскопиясы құрылымды растау және қатты фазалы реакциялардың жүруін бақылау үшін қолданылды.[25] Гордон және басқалар шағын молекулалардың комбинаторлық кітапханаларын құру үшін иминдер мен пептидилфосфонаттарды қолданатын бірнеше жағдайлық зерттеулерді сипаттаңыз.[25] Иминдер кітапханасын құру үшін шайырға байланған амин қышқылы альдегидтің қатысуымен әрекеттеседі. Авторлар реакциялардың жүруін қадағалау үшін жылдам 13 С гельдік фаза NMR спектроскопиясын және 1 H NMR спектроскопияны сиқырлы бұрау әдісін қолданғанын көрсетіп, триметил ортоформатын қолданған кезде бөлме температурасында иминдердің көпшілігін 10 минут ішінде жасауға болатындығын көрсетті. еріткіш. Содан кейін пайда болған иминдер дериватталып, 4-тиазолидинондар, В-лактамдар және пирролидиндер түзілді.
Қатты фазалық тіректерді қолдану қосылыстардың үлкен комбинаториялық кітапханаларының синтезін едәуір жеңілдетеді. Бұл бастапқы материалды қатты тірекке бекіту арқылы, содан кейін жеткілікті үлкен кітапхана салынғанға дейін келесі реакцияларды орындау арқылы жасалады, содан кейін бұйымдар тіректен бөлінеді. Қатты фазаны тазартудың әдісі сұйық-сұйықтық экстракциясын тазартудың стандартты әдістерімен бірге ерітінді-фазалық синтез схемаларында қолдану үшін көрсетілген.
Деконволюция және скрининг
Комбинаторлық кітапханалар
Комбинаторлық кітапханалар - бір сатылы процесте синтезделетін шағын молекулалы химиялық қосылыстардың арнайы көп компонентті қоспалары. Олар жеке қосылыстар жиынтығынан, сондай-ақ параллель синтездеу арқылы дайындалған қосылыстар қатарынан ерекшеленеді, бұл олардың синтезінде қоспалардың қолданылуының маңызды ерекшелігі. Қоспаларды қолдану процестің өте жоғары тиімділігін қамтамасыз етеді. Екі реактор да қоспалар болуы мүмкін және бұл жағдайда процедура одан да тиімді болады. Практикалық себептер бойынша екі қоспаның біреуін бір құрылыс блоктарымен (ББ) алмастыратын сплит-микс әдісін қолданған жөн. Аралас қоспалардың маңыздылығы соншалық, синтезде қоспаны қолданбайтын комбинаторлық кітапханалар болмайды, ал егер қоспада процесте сөзсіз комбинаторлық кітапхана пайда болса. Сплит-микстің синтезі әдетте қатты тіреудің көмегімен жүзеге асырылады, бірақ оны ерітіндіде қолдануға болады. Ол компоненттердің құрылымы болғандықтан деконволюцияның белгісіз әдістерін скринингте қолдану керек, комбинаторлық кітапханалардың маңызды ерекшеліктерінің бірі - бүкіл қоспаны бір процессте экранға шығаруға болады. Бұл кітапханаларды фармацевтикалық зерттеулерде өте пайдалы етеді, сонымен қатар толық комбинаторлық кітапханалардың ішінара кітапханаларын синтездеуге болады. Олардың кейбіреулері деконволюцияда қолданыла алады[26]
Кітапханалардың деконволюциясы берік тіректен шықты
Егер комбинаторлық кітапхананың синтезделген молекулалары қатты тіректен бөлініп алса, еритін қоспасы пайда болады. Мұндай шешімде миллиондаған түрлі қосылыстар табылуы мүмкін. Бұл синтетикалық әдіс дамыған кезде алдымен молекулаларды анықтау және пайдалы қасиеттері бар молекулаларды табу мүмкін емес болып көрінді. Алайда, проблеманы шешу үшін пайдалы компоненттерді анықтау стратегиясы жасалды. Бұл стратегиялардың барлығы ішінара кітапханаларды синтездеуге және тестілеуге негізделген. Ең алғашқы қайталанбалы стратегия Фурканың 1982 ж. Нотариалды куәландырылған жоғарыда аталған құжатында сипатталған.[2]Кейін бұл әдісті Эрб және басқалар дербес жариялады. «рекурсивті деконволюция» атауымен[27]
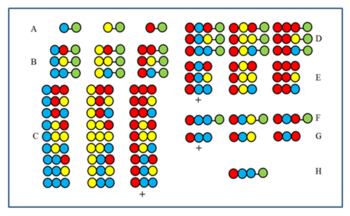
Рекурсивті деконволюция
Әдіс фигура арқылы түсінікті болады. 27 мүше пептидтік кітапхана үш амин қышқылынан синтезделеді. Бірінші (A) және екінші (B) циклдардан кейін үлгілерді оларды араластырмас бұрын бөліп алған. Үшінші циклдің өнімдері (С) араластырылмас бұрын бөлініп алынып, белсенділігі тексеріледі. + Белгісімен белгіленген топ белсенді деп есептейік. Барлық мүшелерде қызыл аминқышқылы соңғы байланыс жағдайында болады (СР). Демек, белсенді мүшеде соңғы CP-де қызыл амин қышқылы болады. Содан кейін қызыл аминқышқылы екінші циклдан кейін бөлінген үш сынамаға қосылады (B) сынамалар алу үшін D. үлгіні алудан кейін үш Е үлгісі түзіледі. Егер сынақтан өткеннен кейін + таңбасы белсенді болса, онда көк аминқышқылының белсенді компоненттегі екінші СР алатындығын көрсетеді. Содан кейін үш А сынамасына алдымен көк, содан кейін қызыл амин қышқылы қосылады (F), содан кейін (G) бөлінгеннен кейін қайтадан сыналады. Егер + компоненті белсенді екенін дәлелдейтін болса, онда белсенді компоненттің реттілігі анықталып, H түрінде көрсетілген.
Позициялық сканерлеу
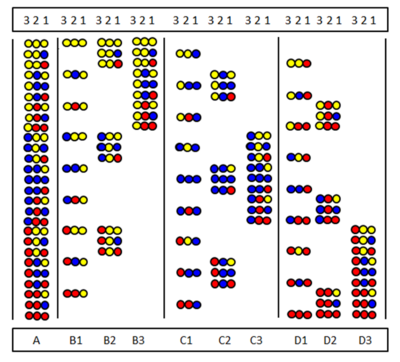
Позициялық сканерлеуді Фурка және басқалар дербес енгізді.[28] және Pinilla және басқалар.[29] Әдіс қосалқы кітапханалар сериясын синтездеуге және тексеруге негізделген. онда белгілі бір дәйектілік позицияны сол аминқышқыл алады. Суретте үш амин қышқылынан жасалған толық пептидтік тримерлер кітапханасының (A) тоғыз кітапханасы (B1-D3) көрсетілген. Кітапханаларда барлық компоненттерде бірдей аминқышқылының орны бар. Кітапхана синтезінде тірек бөлінбейді және тек бір аминқышқылы бүкіл үлгіге қосылады. Нәтижесінде бір позицияны барлық компоненттерде бірдей амин қышқылы алады. Мысалы, В2 кітапханасының 2 жағдайында тоғыз компоненттің барлығында «сары» амин қышқылы бар. Егер скринингтік тестте бұл кіші кітапхана оң жауап берсе, онда белсенді пептидтегі 2-орынды «сары» амин қышқылы да алады деген сөз. Аминқышқылдарының дәйектілігін барлық тоғыз (немесе әлдеқайда аз) кітапханаларды сынау арқылы анықтауға болады.
Кітапханалардан бас тарту
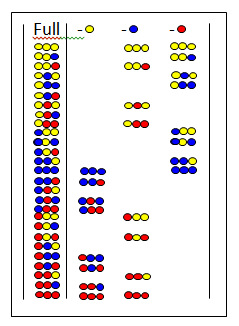
Кітапханаларда жоқ[30][31] қоспаның барлық пептидтерінде белгілі бір амин қышқылы жетіспейді. Суретте толық кітапхана және үш кітапхана жоқ. Жоғарғы жағында алынып тасталған аминқышқылдары көрсетілген. Егер тастап кету кітапханасы теріс сынақ берсе, алынып тасталған амин қышқылы белсенді компонентте болады.
Байланыстырылған комбинаторлық кітапханалардың деконволюциясы
Егер пептидтер қатты тіреуіштен бөлінбесе, біз моншақтардың қоспасымен айналысамыз, әрбір моншақ құрамында жалғыз пептид бар. Смит және оның әріптестері[32] пептидтерді байланыстырылған түрде де тексеруге болатындығын бұрын көрсетті. Бұл тәсіл пептидтік кітапханаларды скринингте де қолданылды. Байланыстырылған пептидтік кітапхана еріген мақсатты протеинмен тексерілді. Ақуыз бекітілген моншақтарды бөліп алып, ақуызды бисерден алып тастады, содан кейін байланған пептидті рет-ретімен анықтады. Біршама өзгеше көзқарасты Тейлор мен Моркен ұстанды.[33] Олар пептидті емес байланыстырылған кітапханалардағы катализаторларды анықтау үшін инфрақызыл термографияны қолданды. Бұл әдіс байланыстырылған кітапхананы субстрат ерітіндісіне батырған кезде катализаторы бар моншақтарда пайда болатын жылуға негізделген. Моншақтарды инфрақызыл микроскоп арқылы зерттегенде моншақтары бар катализатор жарқын дақтар болып көрінеді және оларды таңдауға болады.
Кодталған комбинаторлық кітапханалар
Егер біз пептидті емес органикалық кітапханалар кітапханасымен айналысатын болсақ, онда моншақ құрамының пептидтегідей сәйкестілігін анықтау оңай емес. Осы қиындықты айналып өту үшін моншақтарға қосылу әдістері, кітапхананың синтезімен қатар моншақта түзілген қосылыстың құрылымын кодтайтын молекулалар жасалды. Ольмейер және оның әріптестері екілік кодтау әдісін жариялады[34] Олар 18 тегтеу молекулаларының қоспаларын қолданды, оларды моншақтан айырғаннан кейін Electron Capture Gas Chromatography көмегімен анықтауға болады. Саркар және т.б. жаппай кодталған OBOC кітапханаларын құру үшін қолдануға болатын пентеной амидтерінің (COPAs) хираль олигомерлері сипатталған.[35] Керр және басқалар. кодтаудың инновациялық әдісін енгізді[36] Моншақтарға ортогоналды қорғалатын алынбалы екіфункционалды байланыстырғыш бекітілді. Сілтегіштің бір шеті кітапхананың табиғи емес блоктарын бекіту үшін қолданылған, ал екінші шетіне аминқышқылдарының үштіктерін кодтайтын байланысқан. Құрылыс блоктары табиғи емес аминқышқылдары болды және олардың аминқышқылдарының үштік кодталу қатарын Эдман деградациясы арқылы анықтауға болатын еді. Бұл түрдегі кодтаудың маңызды аспектісі кітапхана мүшелерін моншақтардан және еритін кітапхананы құрайтын кодтау тегтерімен жабу мүмкіндігі болды. Сол тәсілді Николаев және басқалар қолданған. пептидтермен кодтауға арналған.[37] 1992 жылы Бреннер мен Лернер ең табысты кодтау әдісі болып табылатын қатты тіректің моншақтарын кодтау үшін ДНҚ тізбектерін енгізді.[38] Нильсен, Бреннер және Джанда ДНҚ-ны кодтауды жүзеге асыру үшін Керр тәсілін де қолданды[39]Соңғы уақытта ДНҚ секвенциясында маңызды жетістіктер болды. Келесі буын әдістері көптеген үлгілерді қатар тізбектеуге мүмкіндік береді, бұл ДНҚ кодталған кітапханаларды скринингте өте маңызды. ДНҚ-ны кодтаудың сәттілігіне ықпал еткен тағы бір жаңалық болды. 2000 жылы Гальпин мен Харбери ДНҚ кодталған комбинаторлық кітапханалардың сплит-микс синтезіндегі қатты тіректі жіберіп алып, оның орнын кодтаушы ДНҚ олигомерлерімен алмастырды. Қатты фазалық сплит және бассейн синтезінде кітапханалардың құрамдас бөліктерінің саны тіреу моншақтарының санынан аспауы керек. Авторлардың жаңа көзқарасы бойынша бұл ұстамдылық толығымен алынып тасталды және жаңа қосылыстарды іс жүзінде шексіз мөлшерде дайындауға мүмкіндік берді. [40] Мысалы, даттық Nuevolution компаниясы 40 триллионнан тұратын ДНҚ кодталған кітапхананы синтездеді! компоненттер[41]ДНҚ-мен кодталған кітапханалар еритін, бұл скринингте аффинді байланыстыруды тиімді қолдануға мүмкіндік береді. Кейбір авторлар ДНҚ кодталған комбинаторлық кітапханалардың акромиміне DEL қолданады, ал басқалары DECL қолданады. Соңғысы жақсы көрінеді, өйткені осы атаумен аталған кітапханалардың комбинаторлық сипаты айқын көрініс тапқан, ДНҚ-ның кодталған бірнеше типті комбинаторлық кітапханалары қазіргі мыңжылдықтың бірінші онжылдығында енгізілген және сипатталған болатын. Бұл кітапханалар дәрі-дәрмектерді зерттеуде өте сәтті қолданылады.
- 2001 жылы Гартнер және басқалар сипаттаған комбинаториялық кітапханалардың ДНҚ шаблонды синтезі. [42]
- 2004 жылы Mlecco және басқалар ойлап тапқан қос фармакофорлық ДНҚ кодталған комбинаторлық кітапханалар. [43]
- 2004 жылы Harbury Halpin және Harbury шығарған маршруттаудың бірізділігі кодталған. [44]
- 2008 жылы Манокки және басқалар енгізген бірыңғай фармакофорлық ДНҚ кодталған комбинаторлық кітапханалар. [45]
- Ханзен және басқалар жариялаған йоктолитер масштабындағы реакторды қолдану арқылы құрылған ДНҚ кодталған комбинаторлық кітапханалар. 2009 жылы[46]
Оларды синтездеу және қолдану туралы мәліметтер парақта келтірілген ДНҚ-кодталған химиялық кітапхана.ДНҚ кодталған еритін комбинаторлық кітапханалардың кемшіліктері де бар. Бірінші кезекте қатты тіректі қолданудың артықшылығы толығымен жоғалады. Сонымен қатар, ДНҚ-ны кодтайтын тізбектердің полиониялық сипаты синтездегі сулы емес еріткіштердің пайдалылығын шектейді. Осы себепті көптеген зертханалар DECL синтезінде қолдану үшін ДНҚ-мен үйлесімді реакцияларды әзірлеуді таңдайды. Бірнеше қол жетімді сипатталған[47][48][49]
Материалтану
Материалтану жаңа материалдарды ашуда комбинаториялық химия техникасын қолданды. Бұл жұмыс ізашар болды П.Г. Шульц т.б. тоқсаныншы жылдардың ортасында [50] элементтерді кремний субстратына бірге тұндыру арқылы алынған люминесцентті материалдар аясында. Оның жұмысының алдында Дж.Х.Ханак 1970 ж[51] бірақ сол кезде әдістің таралуы үшін компьютер мен робототехника құралдары қол жетімді болмады. Жұмысты бірнеше академиялық топтар жалғастырды[52][53][54][55] сонымен қатар ірі ғылыми-зерттеу және тәжірибелік-конструкторлық бағдарламалары бар компаниялар (Symyx Technologies, GE, Dow химиялық және т.б.). Техника катализ үшін кеңінен қолданылды,[56] жабындар,[57] электроника,[58] және көптеген басқа салалар.[59] Тиісті информатика құралдарын қолдану өндірілген деректердің үлкен көлемін өңдеу, басқару және сақтау үшін өте маңызды.[60] Жаңа түрлері Тәжірибелерді жобалау сонымен қатар комбинаторлық әдістермен күресуге болатын үлкен тәжірибелік кеңістіктерді тиімді шешудің әдістері жасалды.[61]
Әртүрлілікке бағытталған кітапханалар
Комбинаторлық химия жиырма жылдан астам уақыттан бері есірткіні ашудың маңызды бөлігі болғанына қарамастан, FDA клиникалық қолдануға тек бір де-ново комбинаториялық химиямен синтезделген бір ғана химикатты мақұлдады (сорафениб, мультикиназа тежегіші бүйрек қатерлі ісігі үшін көрсетілген).[62] Тәсілдің сәтсіздігін талдау жеткілікті шектеулі байланыстыруға ұсынылды химиялық кеңістік комбинаториялық химия өнімдерімен қамтылған.[63] Комбинаторлық химия кітапханаларындағы қосылыстардың қасиеттерін мақұлданған дәрілік заттармен және табиғи өнімдермен салыстыру кезінде Фехер мен Шмидт[63] комбинациялық химия кітапханалары әсіресе жетіспеушіліктен зардап шегетінін атап өтті ширализм, сонымен қатар құрылымның қаттылығы, олардың екеуі де есірткіге ұқсас қасиеттер ретінде қарастырылады. Табиғи өнім болса да есірткіні табу соңғы уақытта фармацевтикалық индустриядағы ең сәнді тенденция болмады,[дәйексөз қажет ] жаңа химиялық заттардың көп бөлігі табиғаттан алынған қосылыстар болып табылады,[дәйексөз қажет ] Осылайша, скринингтік кітапханалардың химиялық әртүрлілігін арттыру арқылы комбинаториялық химияның тиімділігін арттыруға болады деген ұсыныс жасалды.[64] Хиральділік пен қаттылық - бұл біріктірілген химия кітапханаларындағы мақұлданған дәрілік заттар мен табиғи өнімдерді қосылыстардан ажырататын екі маңызды сипаттама болғандықтан, бұл әртүрлілікке бағытталған кітапханаларда, яғни химиялық кеңістікті қамтуға бағытталған құрама коллекцияларда баса айтылған екі мәселе. көптеген қосылыстардың саны.[дәйексөз қажет ]
Патенттік классификацияның ішкі класы
8-ші басылымында Халықаралық патенттік жіктеу (IPC), 2006 жылдың 1 қаңтарында күшіне енді, арнайы кіші сынып құрылды патенттік өтінімдер және патенттер байланысты өнертабыстар комбинаториялық химия саласында: «C40B».
Сондай-ақ қараңыз
- Комбинаторика
- Химинформатика
- Комбинаторлық биология
- Есірткіні табу
- Динамикалық комбинаториялық химия
- Өткізгіштігі жоғары скрининг
- Математикалық химия
- Молекулалық модельдеу
Әдебиеттер тізімі
- ^ Поттель, Дж .; Moitessier, N. (2017). «Синтетикалық қол жетімді, жергілікті химиялық қосылыстардың теңшелетін генерациясы». Дж.Хем. Инф. Үлгі. 57 (3): 454–467. дои:10.1021 / acs.jcim.6b00648. PMID 28234470.
- ^ а б в Фурка Á. Tanulmány, gyógyászatilag hasznosítható peptidek szisztematikus felkutatásának lehetőségéről (және фармацевтикалық пайдалы пептидтерді жүйелі іздеу мүмкіндігі туралы зерттеу https://mersz.hu/mod/object.php?objazonosito=matud202006_f42772_i2
- ^ Фурка Á (2002). Комбинаторлық химия 20 жыл… Дәрі-дәрмек DiscovToday 7; 1-4.https://doi.org/10.1016/S1359-6446(02)00001-6
- ^ «КОМБИНАТОРЛЫҚ ХИМИЯ: ШОЛУ». Шілде 2013. дои:10.13040 / IJPSR.0975-8232.4 (7) .2502-16. Алынған 21 маусым, 2020.
- ^ Лесни, Марк С. (2002). «Құрама комбинаторлар: химия препаратты дамытуда». Алынған 19 қазан, 2018.
- ^ Джеффри В.Нунан және басқалар. «Тиімді тазарту, кванттау және сипаттама беру әдістері арқылы кітапхана синтезінің параллель шешімін жетілдіру» Зертханалық автоматика журналы, 48 (1992) 3789.
- ^ Е.В.Гордеева және басқалар «COMPASS бағдарламасы - компьютердің көмегімен синтездеудің өзіндік жартылай эмпирикалық тәсілі» Тетраэдр, 48 (1992) 3789.
- ^ Furka Á, Sebestyén F, Asgedom M, Dibó G. Пептидтердің корнукопиясы. Қазіргі заманғы биохимияның маңызды сәттерінде, 14-ші Халықаралық биохимия конгресінің материалдары. VSP.Utrecht.1988; 5; б. 47.
- ^ Á. Фурка, Ф. Себестьен, М. Асгедом, Г. Дибо, көп компонентті пептидті қоспаларды жылдам синтездеудің жалпы әдісі. Int. Дж. Пептидті протеин қоры, 1991, 37, 487-493.
- ^ Merrifield RB, 1963 ж. Am. Хим. Soc. 85, 2149.
- ^ Скотт, Дж .; Смит, Г. (1990-07-27). «Эпитоп кітапханасымен пептидті лигандтарды іздеу». Ғылым. Американдық ғылымды дамыту қауымдастығы (AAAS). 249 (4967): 386–390. дои:10.1126 / ғылым.1696028. ISSN 0036-8075. PMID 1696028.
- ^ Квирла, С. Питерс, Э. А .; Барретт, Р.В .; Дауэр, В. Дж. (1990-08-01). «Фагтағы пептидтер: лигандтарды анықтауға арналған пептидтердің кең кітапханасы». Ұлттық ғылым академиясының материалдары. 87 (16): 6378–6382. дои:10.1073 / pnas.87.16.6378. ISSN 0027-8424. PMC 54537. PMID 2201029.
- ^ Дж. Дж. Девлин, Л. Панганибан және П. Э. Девлин Ғылым 1990, 249, 404.
- ^ Fodor SP, Read JL, Pirrung MC, Stryer L, Lu AT, Solas D, 1991. Жарыққа бағытталған, кеңістіктегі адрестелген параллель химиялық синтез. Ғылым 251, 767-73.
- ^ Х. М. Гейсен, Р. Х. Мелоун, С. Дж. Бартелинг Прок. Натл. Акад. Ғылыми. АҚШ 1984, 81, 3998.
- ^ Э. Дж. Моран, С. Саршар, Дж. Ф. Каргилл, М. Шахбаз, А Лио, А. М. М. Мджалли, Р. В. Армстронг Дж. Ам. Хим. Soc. 1995, 117, 10787.
- ^ K. C. Nicolaou, X –Y. Сяо, З.Парандуш, А.Сеньей, М.П.Нова Анжев. Хим. Int. Ред. Энгл. 1995, 36, 2289.
- ^ Á. Фурка, Дж. В. Кристенсен, Э. Хили, Х.Р. Таннер, Х. Саней Дж. Тарақ Хим. 2000, 2, 220.
- ^ Бут, Р. Джон; Ходжес, Джон С. (1999-2001). «Комбинаторлық синтез өнімдерін жылдам тазартудың қатты-қолдайтын реагенттік стратегиялары». Химиялық зерттеулердің шоттары. 32 (1): 18–26. дои:10.1021 / ar970311n. ISSN 0001-4842.
- ^ Армстронг, Роберт В. Тарақ, Эндрю П .; Темпест, Пол А .; Браун, С.Дэвид; Китинг, Томас А. (1996-2001). «Комбинаторлық кітапхананы синтездеуге арналған көп компонентті конденсация стратегиясы». Химиялық зерттеулердің шоттары. 29 (3): 123–131. дои:10.1021 / ar9502083. ISSN 0001-4842. S2CID 95815562.
- ^ Сонда да, В.Кларк (1996-2001). «Синтетикалық рецепторлардың кодталған комбинаторлық кітапханаларды қолдану арқылы тізбекті-селективті пептидті байланыстыруының ашылуы». Химиялық зерттеулердің шоттары. 29 (3): 155–163. дои:10.1021 / ar950166i. ISSN 0001-4842.
- ^ Дэвит, Шейла Хоббс; Чарник, Энтони В. (1996–2001). «Парке-Дэвистің ДИВЕРСОМЕР әдісін қолданатын комбинациялық органикалық синтез». Химиялық зерттеулердің шоттары. 29 (3): 114–122. дои:10.1021 / ar950209v. ISSN 0001-4842.
- ^ Швабахер, Алан В .; Шэнь, Иксинг; Джонсон, Кристофер В. (1999-2009). «Фурье трансформациясының комбинаториялық химиясы». Американдық химия қоғамының журналы. 121 (37): 8669–8670. дои:10.1021/ja991452i. ISSN 0002-7863.
- ^ Ellman, Jonathan A. (1996–2001). "Design, Synthesis, and Evaluation of Small-Molecule Libraries". Химиялық зерттеулердің шоттары. 29 (3): 132–143. дои:10.1021/ar950190w. ISSN 0001-4842.
- ^ а б Gordon, E. M.; Gallop, M. A.; Patel, D. V. (1996–2001). "Strategy and Tactics in Combinatorial Organic Synthesis. Applications to Drug Discovery". Химиялық зерттеулердің шоттары. 29 (3): 144–154. дои:10.1021/ar950170u. ISSN 0001-4842.
- ^ A. Furka Sub-Library Composition of Peptide Libraries. Potential Application in Screening. Drug Development Research 33, 90-97 (1994).
- ^ Erb E, Janda KD, Brenner S (1994) Recursive deconvolution of combinatorial chemical libraries Proc. Natl Acad Sci.USA 91; 11422-11426.
- ^ Furka Á, Sebestyén F, WC 93/24517, 1993.
- ^ Pinilla C, Appel JR, Blanc P, Houghten RA (1993) Rapid identification of high affinity peptide ligands using positional scanning synthetic peptide combinatorial libraries. BioTechniques 13(6); 901-5.
- ^ Carell TE, Winter A, Rebek J Jr. (1994) A Novel Procedure for the Synthesis of Libraries Containing Small Organic Molecules, Angew Chem Int Ed Engl 33; 2059-2061.
- ^ Câmpian E, Peterson M, Saneii HH, Furka Á, (1998) Deconvolution by omission libraries, Bioorg &[ Med Chem Letters 8; 2357-2362.
- ^ J. A. Smith J. G. R. Hurrel, S. J. Leach A novel method for delineating antigenic determinants: peptide synthesis and radioimmunoassay using the same solid support. Immunochemistry 1977, 14, 565.
- ^ S. J. Taylor, J. P. Morken Thermographic Selection of Effective Catalysts from an Encoded Polymer-Bound Library Science 1998, 280, 267.
- ^ Ohlmeyer MHJ, Swanson RN, Dillard LW, Reader JC, Asouline G, Kobayashi R, Wigler M, Still WC (1993) молекулалық тегтермен индекстелген күрделі синтетикалық химиялық кітапханалар, Proc Natl Acad Sci USA 90; 10922-10926.
- ^ Sarkar M, Pascal BD, Steckler C, Aquino C., Micalizio GC, Kodadek T, Chalmers MJ (1993) Бөлінген және бассейндік комбинаторлық кітапханаларды декодтау, электронды диссоциацияланған тандемді масс-спектрометрия, J Am Soc масс-спектрі 24 (7): 1026- 36.
- ^ Kerr JM, Banville SC, Zuckermann RN (1993) Encoded Combinatorial Peptide Libraries Containing Non-Natural Amino Acids, J Am Chem. Soc 115; 2529-2531.
- ^ Nikolaiev V, Stierandová A, Krchnák V, Seligmann B, Lam KS, Salmon SE, Lebl M, (1993) Peptide-encoding for structure determination of nonsequenceable polymers within libraries synthesized and tested on solid-phase supports, Pept Res. 6(3):161-70.
- ^ Brenner S, Lerner RA. (1992) Encoded combinatorial chemistry. Proc Natl Acad Sci USA 89; 5381–5383.
- ^ Nielsen J, Brenner S, Janda KD. (1993) Synthetic methods for the implementation of encoded combinatorial chemistry. Journal of the American Chemical Society, 115 (21); 9812–9813.
- ^ Harbury DR, Halpin DR (2000) WO 00/23458.
- ^ B. Halford How DNA-encoded libraries are revolutionizing drug discovery. C&EN 2017, 95, Issue 25.
- ^ Gartner ZJ, Tse BN, Grubina RB, Doyon JB, Snyder TM, Liu DR (2004) DNA-Templated Organic Synthesis and Selection of a Library of Macrocycles, Science 305; 1601-1605.
- ^ Melkko S, Scheuermann J, Dumelin CE, Neri D (2004) Nat Biotechnol 22 кодталған өздігінен жиналатын химиялық кітапханалар; 568-574.
- ^ Halpin DR, Harbury PB (2004) DNA Display I. Sequence-Encoded Routing of DNA Populations, PLoS Biology 2; 1015-102.
- ^ Mannocci L, Zhang Y, Scheuermann J, Leimbacher M, De Bellis G, Rizzi E, Dumelin C, Melkko S, and Neri N (2008) High-throughput sequencing allows the identification of binding molecules isolated from DNA-encoded chemical libraries, Proc Natl Acad Sci USA 105;17670–17675.
- ^ Hansen MH, Blakskjær P, Petersen LK, Hansen TH, Højfeldt JW, Gothelf KV, HansenNJV (2009) A Yoctoliter-Scale DNA Reactor for Small-Molecule Evolution (2009) J Am Chem Soc 131; 1322-1327.
- ^ Luk KC, Satz AL (2014) DNA‐Compatible Chemistry in: Goodnow Jr. RA Editor A Handbook for DNA‐Encoded Chemistry: Theory and Applications for Exploring Chemical Space and Drug Discovery, Wiley, pp 67-98.
- ^ Satz AL, Cai J, Chen Y,§, Goodnow R, Felix Gruber F, Kowalczyk A, Petersen A, Naderi-Oboodi G, Orzechowski L, Strebel Q (2015) DNA Compatible Multistep Synthesis and Applications to DNA Encoded Libraries Bioconjugate Chem 26; 1623−1632.
- ^ Li Y, Gabriele E, Samain F, Favalli N, Sladojevich F, Scheuermann J, Neri D (2016) Optimized reaction conditions for amide bond formation in DNA-encoded combinatorial libraries, ACS Comb Sci 18(8); 438–443.
- ^ X. -D. Xiang et al. "A Combinatorial Approach to Materials Discovery" Science 268 (1995) 1738
- ^ Дж. Hanak, J. Mater. Sci, 1970, 5, 964-971
- ^ Combinatorial methods for development of sensing materials, Springer, 2009. ISBN 978-0-387-73712-6
- ^ V. M. Mirsky, V. Kulikov, Q. Hao, O. S. Wolfbeis. Multiparameter High Throughput Characterization of Combinatorial Chemical Microarrays of Chemosensitive Polymers. Macromolec. Rap. Comm., 2004, 25, 253-258
- ^ H. Koinuma et al. "Combinatorial solid state materials science and technology" Sci. Технол. Adv. Mater. 1 (2000) 1 Тегін жүктеу
- ^ Andrei Ionut Mardare et al. "Combinatorial solid state materials science and technology" Sci. Технол. Adv. Mater. 9 (2008) 035009 Тегін жүктеу
- ^ Applied Catalysis A, Volume 254, Issue 1, Pages 1-170 (10 November 2003)
- ^ J. N. Cawse et. al, Progress in Organic Coatings, Volume 47, Issue 2, August 2003, Pages 128-135
- ^ Combinatorial Methods for High-Throughput Materials Science,MRS Proceedings Volume 1024E, Fall 2007
- ^ Combinatorial and Artificial Intelligence Methods in Materials Science II, MRS Proceedings Volume 804, Fall 2004
- ^ QSAR and Combinatorial Science, 24, Number 1 (February 2005)
- ^ J. N. Cawse, Ed., Experimental Design for Combinatorial and High Throughput Materials Development, John Wiley and Sons, 2002.
- ^ D. Newman and G. Cragg "Natural Products as Sources of New Drugs over the Last 25 Years" J Nat Prod 70 (2007) 461
- ^ а б M. Feher and J. M. Schmidt "Property Distributions: Differences between Drugs, Natural Products, and Molecules from Combinatorial Chemistry" J. Chem. Инф. Есептеу. Sci., 43 (2003) 218
- ^ Su QB, Beeler AB, Lobkovsky E, Porco JA, Panek JS "Stereochemical diversity through cyclodimerization: Synthesis of polyketide-like macrodiolides." Org Lett 2003, 5:2149-2152.
Сыртқы сілтемелер
- English version of the 1982 document
- "The concealed side of the history of combinatorial chemistry"
- IUPAC's "Glossary of Terms Used in Combinatorial Chemistry"
- ACS Combinatorial Science (бұрын Journal of Combinatorial Chemistry )
- Combinatorial Chemistry Review
- Molecular Diversity
- Combinatorial Chemistry and High Throughput Screening
- Combinatorial Chemistry: an Online Journal
- SmiLib - A free open-source software for combinatorial library enumeration
- GLARE - A free open-source software for combinatorial library design




