N-гидроксифталимид - Википедия - N-Hydroxyphthalimide
 | |
| Атаулар | |
|---|---|
| IUPAC атауы 2-гидроксизоиндол-1,3-дион | |
| Идентификаторлар | |
3D моделі (JSmol ) | |
| ChemSpider | |
| ECHA ақпарат картасы | 100.007.600 |
| EC нөмірі |
|
PubChem CID | |
| UNII | |
CompTox бақылау тақтасы (EPA) | |
| |
| |
| Қасиеттері | |
| C8H5NO3 | |
| Молярлық масса | 163.132 г · моль−1 |
Өзгеше белгіленбеген жағдайларды қоспағанда, олар үшін материалдар үшін деректер келтірілген стандартты күй (25 ° C [77 ° F], 100 кПа). | |
| Infobox сілтемелері | |
N-Гидроксифталимид болып табылады N-гидрокси туындысы фталимид. Қоспа қолданылады, басқалармен қатар, сияқты катализатор үшін тотығу реакциялары, атап айтқанда селективті тотығу үшін (мысалы, g. алкандар дейін алкоголь ) бірге молекулалық оттегі жұмсақ жағдайда.[1][2]
Пайда болуы және өндірісі
Синтезі N-гидроксифталимид фталатил хлориді және гидроксиламин гидрохлориді натрий карбонатының қатысуымен сулы ерітіндіде алғаш рет 1880 жылы Лассар Кон хабарлаған («Фталилгидроксиламин» деп аталады).[3]
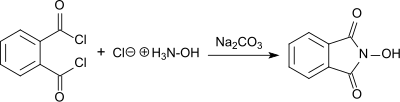
Өнім қызыл түрінде пайда болады натрий тұзы ақ, ал негізгі жағдайларда N-гидроксифталимид ерітіндіге сәйкес 55% өнімде тұнбаға түседі қышқылданған. N-гидроксифталимид гидроксиламин гидрохлоридін реакцияға түсіру арқылы да өндіріледі диетилфталат қатысуымен натрий ацетаты,[4] немесе бірге фталь ангидриді қатысуымен натрий карбонаты жылытумен. Соңғы жағдайда тазартудан кейін жалпы кірістілік 76% құрайды қайта кристалдандыру.[5]
Фтал ангидриді мен гидроксиламин гидрохлоридінің микротолқынды сәулеленуі пиридин өндіреді N-гидроксифталимид 81% кірістілікте.[6] Негіз болмаған кезде де фтал ангидриді мен гидроксиламин фосфаты реакцияға түсіп, түзіледі. N-гидроксифталимид 86% өнімділікпен 130 ° C дейін қыздырғанда.[7]

Қасиеттері
N-Гидроксифталимид - бұл суда және органикалық еріткіштерде еритін түссізден сарыға дейін, иіссіз кристалды ұнтақ. сірке қышқылы, этил ацетаты және ацетонитрил.[8] Қосылыс екі түрлі түсті болады моноклиникалық кристалдар түзеді. Түссіз ақ түсті жағдайда N-OH тобы молекула жазықтығынан шамамен 1,19 ° айналады, ал сары түрінде ол планарлыққа едәуір жақын (айналу 0,06 °).[9]
Синтезделген түс N-гидроксифталимид қолданылатын еріткіштің түріне байланысты; түстің ақтан сарыға ауысуы қайтымсыз.[10] N-гидроксифталимид қатты түсті, көбінесе сары немесе қызыл тұздар түзеді сілтілік және ауыр металдар, аммиак және аминдер.[11] Гидролиз N-гидроксифталимид күшті негіздер қосу арқылы фтал қышқылын моно түзедігидроксамин қышқылы арқылы су қосу көміртек-азоттық байланыстардың бірінде.[4] N-гидроксифталимид эфирлері, керісінше, түссіз және қамтамасыз етеді O-алкилгидроксиламиндер сілтілік гидролиз немесе бөлшектеу жолымен гидразин гидраты.
Кон хабарлаған «фталилгидроксиламиннің» а бар екендігі белгілі болды молекулалық формула туралы C
8H
5ЖОҚ
3 бірақ нақты құрылымы белгісіз болды.[3] Үш мүмкіндік талқыланды және төмендегі суретте көрсетілген: моно-оксим фталь ангидриді («фталоксим», Мен), кеңейтілген екі гетероатомды сақина, (2,3-бензоксазин-1,4-дион, II), және N-гидроксифталимид (III).[10][12] 1950 жылдарға дейін ғана Кон өнімі (III), N-гидроксифталимид.[13]

Қолдану және реакциялар
Нефкенс пен Тессер генерациялау техникасын жасады белсенді эфирлер бастап N-гидроксифталимид[14] пайдалану үшін пептидтік синтез,[15] кейінірек қолдануға кеңейтілген тәсіл N-гидроксисуцинимид.[16] Эфирлік байланыс арасында қалыптасады N-гидроксифталимид және а карбон қышқылы арқылы жою судың қосындысы N,N '-дициклогексилкарбодиимид (DCC). Пептидтер синтезі үшін N- өсіп келе жатқан пептидтің терминусы қорғалған бірге терт-бутилоксикарбонил ал оның C-терминус (Z-NH-CH (R) -COOH) байланысады N-гидроксифталимид. Ан күрделі эфир келесі амин қышқылы қажетті пептидтік тізбекте активтендірілген эфирмен шайқалып, тізбекке қосылып, ығысады N-гидроксифталимид. Бұл реакция сандық және дерлік 0 ° C температурада болады.[15][17] Алынған эфирді цикл қайталанбас бұрын гидролиздеу керек.

The N-гидроксифталимидті шайқау арқылы жоюға болады натрий гидрокарбонаты,[15] Бірақ N-гидроксисуцинимидтің тәсілі үлкен реактивтілік пен ыңғайлылықты көрсетеді және әдетте басымдыққа ие.[16][17]
Эстер N-гидроксифталимид және активтендірілген сульфон қышқылдары сияқты трифторометансульфонды ангидрид немесе р-толуэнсульфонилхлорид ультрафиолет сәулелену кезінде протондарды бөліп алатын фото қышқылдар деп аталады.

Протондар қышқылға сезімтал жергілікті деградацияға қызмет етеді фоторезистер.[18]
N-гидроксифталимидті палладий (II) ацетаты болған кезде винилацетатпен айналдыруға болады N-винилоксифталимид, ол сандық гидрирленген N-этоксифталимид және декольте арқылы тазартылғаннан кейін, өнімділік O-этилгидроксиламин.[19]

Әр түрлі функционалды топтарды тотығуға болады аминоксил радикалы (фталимид-N-оксил, PINO)[20] бастап сутегі атомын абстракциялау арқылы пайда болды N-гидроксифталимид жұмсақ жағдайда (ұқсас TEMPO ):[1]
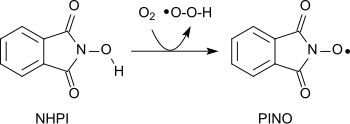
Молекулалық оттегі алкандарының көмегімен тотығып, спирттер, екінші реттік спирттерді кетондарға, ацеталдарды күрделі эфирлерге, алкендерді эпоксидтер.[21][22][23] Амидтер көмегімен карбонилді қосылыстарға айналуы мүмкін N-гидроксифталимид және кобальт (II) тұздары жұмсақ жағдайда.[24]

Маңызды негізгі химиялық заттардың ізашарларының тотығу реакцияларының тиімділігі ерекше техникалық қызығушылық тудырады. Мысалға, ε-капролактам циклогександы тотықтыру кезінде алынған КА майынан («кетон-спирт» майы, циклогексанол мен циклогексанон қоспасы) NHPI қолдану арқылы дайындалуы мүмкін. Реакция циклогексанол гидропероксиді арқылы жүреді, ол аммиакпен әрекеттесіп, пероксидициклогексиламин береді, содан кейін литий хлориді каталитикалық мөлшерде болғанда қайта түзіледі.[22][25]

Пайдалану N-Гидроксифталимид КА майының тотығуындағы катализатор ретінде әдеттегі ε-капролактам синтезімен өндірілетін жағымсыз жанама аммоний сульфатының түзілуіне жол бермейді (Бекманды қайта құру циклогексанон оксимінің күкірт қышқылы ).
Алкандар азот диоксиді болған кезде нитроалканға айналады.[26]
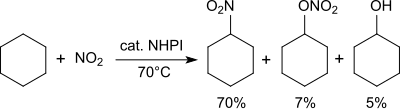
Циклогексан азот диоксиді / ауамен 70 ° C температурада нитроциклогексан (70%), циклогексил нитраты (7%) және циклогексанол (5%) қоспасына айналады.
Сонымен қатар N-гидроксифталимид тотықтырғыш ретінде фотографтар[27] және тонердегі зарядты бақылау агенттері ретінде[28] патенттік әдебиетте сипатталған.
Фталимидо-N-оксил (PINO)
Н-атомын жою арқылы алынған радикал N-гидроксифталимид деп аталады N-фталимидо-N-оксил, қысқартылған болу PINO. Бұл қуатты Н-атомды абстракциялаушы агент.[1] NHPI байланысының диссоциациялану энергиясы (яғни, PINO-H) еріткішке байланысты 88-90 ккал / моль аралығында болады.[29]
Әдебиеттер тізімі
- ^ а б в Рекуперо, Франческо; Пунта, Карло (2007). «Органикалық қосылыстардың радикалды функционализациясын катализатор N-Гидроксифталимид ». Хим. Аян 107 (9): 3800–3842. дои:10.1021 / cr040170k. PMID 17848093.
- ^ Қауын, Люцио; Пунта, Карло (2013). «Металлсыз аэробты тотығу N-гидроксифталимид. Қысқаша шолу ». Beilstein J. Org. Хим. 9: 1296–1310. дои:10.3762 / bjoc.9.146. PMID 23843925.
- ^ а б Кон, Лассар (1880). «Фталилгидроксиламин: Ueberführung der Phthalsäure in Salicylsäure» [N-гидроксифталимид: фтал қышқылының салицил қышқылына айналуы]. Джастус Либигс Анн. Хим. (неміс тілінде). 205 (3): 295–314. дои:10.1002 / jlac.18802050304.
- ^ а б Бауэр, Людвиг; Миарка, Стэнли В. (1957). «Химия N-Гидроксифталимид ». Дж. Хим. Soc. 79 (8): 1983–1985. дои:10.1021 / ja01565a061.
- ^ Гросс, Х .; Keitel, I. (1969). «Zur Darstellung von N-Гидроксифталимид және т.б. N-Гидроксисуцинимид »[дайындау туралы N-гидроксифталимид және N-гидроксисуцинимид]. Дж. Практ. Хим. (неміс тілінде). 311 (4): 692–693. дои:10.1002 / prac.19693110424.
- ^ Сугамото, Казухиро; Мацусита, Ёх-ичи; Камеда, Юй Хей; Сузуки, Масахико; Мацуи, Таканао (2005). «Микротолқынды синтез N‐Гидроксифталимид туындылары ». Синт. Коммун. 35 (1): 67–70. дои:10.1081 / SCC-200046498.
- ^ БӨ қосымшасы 1085013, Elke Fritz-Langhals, «Verfahren zur Herstellung велосипедшісі N-Гидрокси-дикарбоксимид (Циклды дайындау процесі N-hydroxydicarboximides) «, 2001-03-21 жарияланған, Consortium für elektrochemische Industrie GmbH
- ^ Гамбаротти, Кристиан; Пунта, Карло; Рекуперо, Франческо; Злоторзинска, Мария; Саммис, Гленн (2013). «N-гидроксифталимид». N-Гидрофталимид. Органикалық синтезге арналған реагенттер энциклопедиясы. дои:10.1002 / 047084289X.rn00598.pub2. ISBN 978-0471936237.
- ^ Рейхелт, Хендрик; Фонс, Честер А .; Paradies, Henrich H. (2007). «. Қолданылмайтын нысандары мен құрылымдары N-гидроксифталимид: -нің түссіз және сары кристалды формалары N-гидроксифталимид ». J. физ. Хим. A. 111 (13): 2587–2601. дои:10.1021 / jp068599y. PMID 17388355.
- ^ а б Эмс, Д. Е .; Сұр, Т.Ф. (1955). «N-Гидрокси-имидтер. II бөлім. Гомофтальды және фтал қышқылының туындылары ». Дж.Хем. Soc.: 3518–3521. дои:10.1039 / JR9550003518.
- ^ Порчедду, Андреа; Джакомелли, Джампаоло (2009). «Оксимдер мен гидроксамикалық қышқылдардың синтезі». Рапапортта, Zvi; Либерман, Джоэль Ф. (ред.) Гидроксиламиндер, оксимдер және гидроксамикалық қышқылдар химиясы, 1 бөлім. Чичестер: Вили. 224–226 бет. ISBN 978-0-470-51261-6.
- ^ Брэдли, Оскар Л. Бейкер, Лесли С .; Голдштейн, Ричард Ф .; Харрис, Сэмюэль (1928). «LXVIII. — Оксимдердің изомериясы. ХХХІІІ бөлім. Опиан қышқылы мен фтал ангидридінің оксимдері». Дж.Хем. Soc.: 529–539. дои:10.1039 / JR9280000529.
- ^ Херд, Чарльз Д .; Бьюс, Чарльз М .; Бауэр, Людвиг (1954). «Сукчино- және фтало-гидроксамикалық қышқылдар». Дж. Орг. Хим. 19 (7): 1140–1149. дои:10.1021 / jo01372a021.
- ^ Нефкенс, Г. Х. Л .; Тессер, Г.И .; Нивард, R. J. F. (1962). «Эфирлерінің синтезі мен реакциясы N-гидроксифталимид және N-қорғалған аминқышқылдары ». Ескерту. Трав. Хим. Пейс-Бас. 81 (8): 683–690. дои:10.1002 / recl.19620810807.
- ^ а б в Нефкенс, Г. Х. Л .; Tesser, G. I. (1961). «Пептид синтезіндегі романның белсенді етері». Дж. Хим. Soc. 83 (5): 1263. дои:10.1021 / ja01466a068.
- ^ а б Андерсон, Джордж В .; Циммерман, Джоан Э .; Каллахан, Фрэнсис М. (1964). «Эфирлерін қолдану N-Пептид синтезіндегі гидроксисуцинимид ». Дж. Хим. Soc. 86 (9): 1839–1842. дои:10.1021 / ja01063a037.
- ^ а б Боданский, Миклош (1993). «Іске қосу және байланыстыру». Пептидтер синтезінің принциптері (2-ші басылым). Шпрингер-Верлаг. 9-61 бет. дои:10.1007/978-3-642-78056-1_2. ISBN 9783642780561.
- ^ 0919867, К.Элиан, Э.Гюнтер, Р.Лейшнер
- ^ 1995025090, D.M.C. Каллант, AMC.F. Кастелижнс, Дж. Де Фриз
- ^ С. Козери (2009), «Фталимид ‐ N ‐ оксил (PINO) радикалы, күшті каталитикалық агент: оның пайда болуы және әр түрлі органикалық субстратқа қатысты жан-жақтылығы», Катал. Аян. Eng., 51 (2), 218–292 б., дои:10.1080/01614940902743841
- ^ Ю. Ишии, К. Накаяма, М. Такено, С. Сакагучи, Т. Ивахама, Ю. Нишияма (1995), «Роман Катализі N- Органикалық субстраттардың молекулалық оттегімен тотығуындағы гидроксифталимид », Дж. Орг. Хим., 60 (13), 3934–3935 б., дои:10.1021 / jo00118a002CS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме)
- ^ а б «Көміртекті радикалды өндіруші катализатордың ашылуы және оны органикалық синтезге қолдану» (PDF). TCIMAIL, 116 нөмірі. Токио Химиялық Индустрия Лтд., Сәуір 2003 ж. Алынған 2016-08-11.
- ^ Б.Б.Вентцель, М.П.Ж. Донерлер, П.Л. Альстер, М.С. Feiters, R.J.M. Nolte (2000), «N-Гидроксифталимид / кобальт (II) молекулалық оттегін пайдаланып төмен температуралы бензилді тотығуды катализдейді », Тетраэдр, 56 (39), 7797–7803 б., дои:10.1016 / S0040-4020 (00) 00679-7CS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме)
- ^ Ф.Минисчи, К.Пунта, Ф. Рекуперо, Ф. Фонтана, Г.Ф. Педулли (2002), «Аэробты тотығу N-Алкиламидтер катализдейді N-Гидроксифталимид жеңіл жағдайда. Полярлық және энтальпиялық әсерлер », Дж. Орг. Хим., 67 (8), 2671-2676 б., дои:10.1021 / jo016398e, PMID 11950315CS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме)
- ^ О.Фукуда, С.Сакагучи, Ю.Ишии (2001), «Каталитикалық Байер-Виллигер тотығуының KA-майын молекулалық оттегімен пайдаланып тотықтырудың жаңа стратегиясы N-гидроксифталимид », Тетраэдр Летт., 42 (20), 3479–3481 бб, дои:10.1016 / S0040-4039 (01) 00469-5CS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме)
- ^ С.Сакагучи, Ю.Нишиваки, Т.Китамура, Ю.Ишии (2001), «NO2-мен ауанның көмегімен катализаторлық алканды тиімді нитрлеу N-гидроксифтальмид », Angew. Хим., Инт. Өңдеу., 40 (1), 222-224 б., дои:10.1002 / 1521-3773 (20010105) 40: 1 <222 :: AID-ANIE222> 3.0.CO; 2-WCS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме)
- ^ БӨ қосымшасы 0664479, В.Ишикава және Т.Сампей, 1994-7-26 жж. Жарияланған Konica Corp.
- ^ АҚШ 5332637, Дж. Уилсон; С.М. Bonser & H.W. Osterhoudt, «Электростатографиялық құрғақ тонер және гидроксифталимидпен әзірлеуші композициялар», 1994-7-26 жылдары шығарылған, Eastman Kodak Co.
- ^ Coseri, Sergiu (2009). «Фталимид ‐ N ‐ оксил (PINO) радикалы, қуатты каталитикалық агент: оның генерациясы және әр түрлі органикалық субстраттарға қатысты жан-жақтылығы». Катализге арналған шолулар. 51 (2): 218–292. дои:10.1080/01614940902743841.
