Эболаға қарсы вакцина - Ebola vaccine
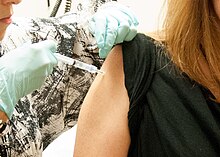 Үміткер Эболаға қарсы вакцина беріліп жатыр | |
| Вакцинаның сипаттамасы | |
|---|---|
| Мақсатты ауру | Эбола вирусы |
| Түрі | Әлсіреген вирус |
| Клиникалық мәліметтер | |
| Сауда-саттық атаулары | Эрвебо, Забдено, Мвабеа |
| ATC коды | |
| Құқықтық мәртебе | |
| Құқықтық мәртебе |
|
Эболаға қарсы вакциналар болып табылады вакциналар немесе мақұлданған немесе алдын-алу үшін әзірлеуде Эбола. Құрама Штаттарда мақұлданған алғашқы вакцина болды rVSV-ZEBOV 2019 жылдың желтоқсанында.[1][2] Бұл кеңінен қолданылған Киву Эбола эпидемиясы астында мейірімді пайдалану хаттама.[3] ХХІ ғасырдың басында бірнеше вакцинаға үміткерлер адамгершілікке жатпайтын приматтарды қорғау тиімділігін көрсетті (әдетте макакалар ) өлімге әкелетін инфекцияға қарсы.[4][5][6]
Вакциналарға жатады шағылыстыру - жетіспейтін аденовирус реплика-құзыретті векторлар везикулярлық стоматит (VSV) және адамның парагриппі (HPIV-3) векторлары және вирусқа ұқсас нанобөлшек дайындық. Иммунизациядан кейін адамның қоздырғышқа әсер ету тиімділігін зерттеуге арналған әдеттегі сынақтар бұл жағдайда этикалық емес. Мұндай жағдайлар үшін АҚШ Азық-түлік және дәрі-дәрмектерді басқару (FDA) «жануарлардың тиімділігі ережесі «негізінде лицензияны бекітуге мүмкіндік береді жануарлар моделі қауіпсіздіктің және әлеуетті әсер етудің дәлелдерімен біріктірілген адам ауруын қайталайтын зерттеулер иммундық жауап вакцина берген адамдардан (қандағы антиденелер). Клиникалық зерттеулер иммундық реакцияны бағалау, кез-келген жанама әсерлерін анықтау және тиісті мөлшерін анықтау үшін сау адамдарға сынамалы вакцинаны енгізу.[7]
Бекітілген
rVSV-ZEBOV
VSV-EBOV немесе rVSV-ZEBOV, Ervebo сауда маркасымен сатылатын, вакцина везикулярлық стоматит бетті білдіру үшін генетикалық түрлендірілген вирус гликопротеин туралы Эбола Заир вирусы.[8][9] 2019 жылдың қарашасында Еуропалық Комиссия шартты маркетингтік рұқсат берді.[10] ДДСҰ алдын-ала біліктілігі 48 сағаттан аз уақыттан кейін келді, бұл вакцинаға дейінгі біліктіліктің ДДҰ жүргізген ең жылдам процесі болды.[11] Ол Еуропалық Одақта медициналық қолдануға 2019 жылдың қарашасында мақұлданды.[12] Ол АҚШ-та медициналық пайдалануға 2019 жылдың желтоқсанында мақұлданды.[1][13]
Ең жиі кездесетін жанама әсерлерге ауырсыну, инъекция аймағында ісіну және қызару, бас ауруы, безгегі, бұлшықет ауыруы, шаршау және буын ауруы жатады.[12] Жалпы алғанда, бұл реакциялар вакцинациядан кейін жеті күн ішінде пайда болады, қарқындылығы жеңіл және орташа және бір аптадан аз уақытта шешіледі.[12]
Оны әзірледі Канада денсаулық сақтау агенттігі, кейіннен даму қолға алынды Merck Inc.[14] 2014 жылдың қазанында Жақсы сенім ол Ұлыбританияның ең ірі құрылтайшыларының бірі болды,[15] Еуропадағы, Габондағы, Кениядағы және АҚШ-тағы сау еріктілерге арналған бірнеше сынақтар басталғанын хабарлады.[16] Вакцина Солтүстік Америкада, Еуропада және Африкада бірнеше жерлерде қауіпсіз екендігі дәлелденді, бірақ Швейцарияның Женева қаласындағы бір сынақ алаңында бірнеше еріктілер шамамен екі аптадан кейін вакцинамен байланысты артрит дамыды, ал есеп беру орындарындағы еріктілердің шамамен 20-30%. вакцинадан кейінгі төмен деңгейлі безгегі дамыды, ол бір-екі күнде шешілді. Басқа жиі кездесетін жанама әсерлері инъекция орнындағы ауырсыну, миалгия және әлсіздік болды.[17] Сынақ ықтимал жағымсыз әсерлерге байланысты 2014 жылдың желтоқсанында уақытша тоқтатылды, бірақ кейіннен қайта жалғасты.[18] 2015 жылдың сәуір айындағы жағдай бойынша[жаңарту], VSV-EBOV бір реттік дозасы бар III фазалық сынақ Батыс Африка елінде II кезеңнің сәтті зерттеуінен кейін Либерияда басталды.[19] 2015 жылдың 31 шілдесінде Гвинеядағы ІІІ кезеңдегі сынақтың алдын ала нәтижелері вакцинаның «өте тиімді және қауіпсіз» болып шыққанын көрсетті.[20] Сот отырысы а сақиналық вакцинация Эбола инфекциясының жаңа жағдайларының ең жақын контактілеріне бірінші немесе бірден немесе 21 күннен кейін вакцина егілген хаттама. Жедел вакцинацияның тиімділігі көрсетілгендіктен, барлық алушылар дереу иммундаудан өтеді.[21][22] Сақинаға қарсы вакцинация - бұл бағдарламада жою әдісі шешек 1970 жылдары. Сынақ вакцинаның құруда тиімді екендігіне баға беруді жалғастырады табын иммунитеті Эбола вирусын жұқтыруға дейін.[23] 2016 жылдың желтоқсанында жүргізілген зерттеу нәтижесінде VSV-EBOV вакцинасы Эбола вирусына қарсы 95-100% тиімді болды, бұл ауруға қарсы алғашқы дәлелденген вакцина болды.[24][25][26]
Бұл мақұлдау Гвинеяда жүргізілген зерттеу барысында қолдау тапты 2014–2016 жұқпалы ауру 18 жастан асқан адамдарда.[1] Зерттеу рандомизирленген кластерлік (сақиналы) вакцинациялау зерттеуі болды, онда лабораторияда расталған Эбола вирусы (EVD) бар адамдардың 3537 контактілері және контактілері, «жедел» немесе 21 күндік «кешіктірілген» вакцинация алынды.[1] Бұл дизайн пациент симптоматикалық уақыт өткізген тұрғын үйлерді немесе жұмыс орындарын немесе сол адамның ауруы немесе қайтыс болуы кезінде науқаспен байланыста болған жеке адамдардың үйін немесе мекен-жайларын қамтуы мүмкін адамдардың әлеуметтік желісін алуға бағытталған.[1] EVD жағдайларын «жедел» вакцинациялау қолындағы 2 108 адам мен «кешіктірілген» вакцинация қолындағы 1429 адам арасында салыстыра отырып, Ervebo вакцинациядан кейін он күннен кейін симптомдар басталған Эбола жағдайларын болдырмауға 100% тиімді екендігі анықталды.[1] 21 күндік «кешіктірілген» кластерлік топтағы EVD он жағдайымен салыстырғанда, «жедел» кластерлік топта вакцинациядан кейін он күннен асқан симптомның басталуымен EVD жағдайлары байқалған жоқ.[1]
Қосымша зерттеулерде антиденелердің реакциясы Либерияда 477 адамда, Сьерра-Леонеде 500 адамда және Канадада, Испанияда және АҚШ-та шамамен 900 адамда бағаланды.[1] Канадада, Испанияда және АҚШ-та жүргізілген зерттеудегі антиденелердің жауаптары Либерия мен Сьерра-Леонда жүргізілген зерттеулердегі адамдарға ұқсас болды.[1]
Қауіпсіздік Африкада, Еуропада және Солтүстік Америкада шамамен 15000 адамда бағаланды.[1] Көбінесе жанама әсерлер инъекция аймағында ауырсыну, ісіну және қызару, сонымен қатар бас ауруы, безгегі, буындар мен бұлшықеттердің ауыруы және шаршау болды.[1]
2016 жылдың желтоқсан айында жүргізілген зерттеу нәтижесінде VSV-EBOV вакцинасы Эбола вирусына қарсы 70-100% тиімді болып шықты, бұл ауруға қарсы алғашқы дәлелденген вакцина болды.[24][25][26] Алайда, осы зерттеудің дизайны мен вакцинаның жоғары тиімділігі күмәнданды.[27] 2019 жылдың қарашасында Еуропалық Комиссия Эрвебоға шартты маркетингтік рұқсат берді (rVSV∆G-ZEBOV-GP, тікелей эфир)[28] және ДДҰ Эболаға қарсы вакцинаны бірінші рет алдын-ала дайындады.[11]
Ad26.ZEBOV / MVA-BN-Filo
Zabdeno және Mvabea сауда маркаларымен сатылатын Ad26.ZEBOV және MVA-BN-Filo екі дозалы режимі,[29][30] әзірлеген Джонсон және Джонсон оның жанында Янсен фармацевтика компания. Ол Еуропалық Одақта медициналық қолдануға 2020 жылдың шілдесінде мақұлданды.[31][29][30]
Режим екі вакцинаның құрамдас бөлігінен тұрады (бірінші вакцина негізгі, содан кейін екінші вакцина күшейту )[32] - бірінші AdVac технологиясына негізделген Крюселл Бастап MVA-BN технологиясына негізделген Holland B.V. (Янсеннің құрамына кіреді) Бавариялық скандинавия. Ad26.ZEBOV адамның аденовирустық 26 серотипінен (Ad26) алынған, эбола вирусын шығаратын Mayinga варианты гликопротеин, ал екінші компонент MVA-BN - Модификацияланған вакциналық вирус Анкара - Бавариялық скандинавиялық (MVA-BN) фило-вектор.[33] Бұл өнім I кезеңнен басталды клиникалық сынақ кезінде Дженнер институты 2015 жылдың қаңтарында Оксфордта.[34][35] Алдын-ала алынған мәліметтер вакцинаның негізгі күшейтілген режимі еріктілерде вакцинациядан күткендей уақытша иммунологиялық реакция тудырғанын көрсетті. Екінші кезеңдегі сынақ 612 ересек ерікті қабылдады және 2015 жылдың шілдесінде Ұлыбритания мен Францияда басталды. Африкада 1200 ерікті қамтыған екінші фазалық сынақ басталды[32] бірінші сот ісі 2015 жылдың қазан айында Сьерра-Леонеде басталды.[36]
2019 жылдың қыркүйегінде Адамға арналған дәрілік заттар комитеті (CHMP) Еуропалық дәрі-дәрмек агенттігі (EMA) Янсенге Ad26.ZEBOV және MVA-BN-Filo үшін жеделдетілген баға берді,[37] және 2019 жылдың қарашасында Янсен а Маркетингті авторизациялау туралы өтініш (MAA) Ad26.ZEBOV және MVA-BN-Filo мақұлдау үшін EMA-ге.[37][38]
2020 жылдың мамырында EMA CHMP Ad26.ZEBOV (Zabdeno) және MVA-BN-Filo (Mvabea) вакциналарын біріктіруге маркетингтік рұқсат беруді ұсынды.[39][40][41] Алдымен Забдено беріледі, ал Мвабеа сегіз аптадан кейін күшейткіш ретінде енгізіледі.[39] Бұл екі дозалы профилактикалық режим жедел қорғаныс қажет болған кезде эпидемияға жауап беру үшін жарамсыз.[39] Жақында Эбола вирусына шалдығу қаупі бар адамдарға (мысалы, денсаулық сақтау мамандары және Эбола вирусы дамып келе жатқан аудандарда тұратын немесе баратын адамдар үшін) сақтық шарасы ретінде, Забденоны аяқтаған адамдар үшін қосымша Забдено үдеткіш вакцинасы қарастырылуы керек. Мвабеаға вакцинацияның екі дозалық режимі төрт айдан астам уақыт бұрын.[39] Адамдар үшін тиімділігі әлі белгілі емес, өйткені тиімділігі жануарларды зерттеу нәтижесінде экстраполяцияланған.[42]
Дамуда
| Қатысты мақалалар |
| Батыс Африка Эбола вирусының эпидемиясы |
|---|
 |
| Шолу |
| Кең таралған жағдайлары бар халықтар |
| Басқа зардап шеккен халықтар |
| Басқа ошақтар |
| Вакцина | Қауымдастырылған ұйымдар | Күй |
|---|---|---|
| Химп аденовирусы 3 векторлы гликопротеин (cAd3-EBO Z) | GSK & NIAID | III кезең 2016 жылғы ақпан[7] |
| rVSV векторлы гликопротеин (VSV-EBOV) | Newlink Genetics & Мерк | Қолдануда[43][44][28][1] |
| Адам аденовирусы 5 векторлы 2014 гликопротеинді кірістіру (Ad5-EBOV) | BIT & CanSino | I кезең аяқталды[45] |
| Аденовирус 26 векторлы гликопротеин / MVA-BN (Ad26.ZEBOV / | Джонсон және Джонсон | Қолдануда[33][46] |
| HPIV-3 векторлы гликопротеин | Денсаулық сақтау министрлігі (Ресей) | I кезең жоспарланған[47] |
| Құтыру векторлы гликопротеин | Томас Джефферсон университеті & NIAID | Адамзатқа жат приматтардың қиындықтары аяқталды[48] |
| Тазартылған гликопротеин | Ақуыз туралы ғылымдар | NHP проблемасы басталды[49] |
| Эбола ∆VP30 H2O2 өңделген | Висконсин университеті | Адамзатқа жат приматтардың қиындықтары аяқталды[50] |
cAd3-EBO Z
2014 жылдың қыркүйегінде вакцинаға арналған І кезеңнің екі клиникалық сынақтары басталды cAd3-EBO Z, ол шимпанзенің әлсіреген нұсқасына негізделген аденовирус (cAd3) генетикалық өзгеріске ұшыраған, сондықтан оны адамдарда көбейту мүмкін емес.[51] CAd3 векторында Эбола вирусының гликопротеинін кодтайтын ДНҚ-фрагменті бар, ол вирионның бетінде көрінеді және хост жасушаларына қосылу және мембраналық синтездің катализі үшін өте маңызды.[52] Ол әзірледі NIAID Okairos-пен бірлесіп, қазір GlaxoSmithKline. VRC 20 тағайындалған сынақ үшін Мэриленд штатындағы Бетезда қаласында NIAID 20 ерікті қабылдады, ал әрқайсысы 20 волонтерден тұратын үш доза тобы EBL01 сынағына Ұлыбритания Оксфорд Университеті қабылдады. Бастапқы нәтижелер 2014 жылдың қараша айында шығарылды; барлық 20 еріктілерде Эболаға қарсы антиденелер жасалды және қауіпсіздікке қатысты ешқандай алаңдаушылық болған жоқ.[53][54] 2014 жылдың желтоқсанында Оксфорд университеті MVA-BN негізіндегі вакцина вакцинасын енгізу үшін сынақты кеңейтті, штамм Анкара вакцинасы өзгертілді, әзірлеген Бавариялық скандинавия, бұл иммундық реакцияларды одан әрі арттыруға көмектесе алатынын зерттеу.[55][56] Барлығы 60 ерікті қатысқан сот процесі вакцинамен вакциналанған 30 ерікті көреді. 2015 жылдың сәуір айындағы жағдай бойынша[жаңарту], CAd3-EBO Z бір дозасымен III фазалық сынақ Батыс Африка елдерінде 2-кезеңді оқудан кейін Сьерра-Леонда басталады.[19][57]
Эбола GP вакцинасы

Филадельфиядағы 8-ші вакцина мен ISV конференциясында 2014 ж. 27-28 қазанында, Новавакс Inc «бірнеше аптада» даму туралы хабарлады гликопротеин (Жалпы дәрігер) нанобөлшек Эбола вирусына қарсы вакцина (EBOV GP) олардың меншігін қолданады рекомбинантты технология. Рекомбинантты ақуыз - бұл коды тасымалданатын ақуыз рекомбинантты ДНҚ. Вакцина жаңадан жарияланған генетикалық дәйектілікке негізделген[58] 2014 ж Гвинея Эболасы (Makona) штамм, ол Батыс Африкада 2014 жылы Эбола ауруының эпидемиясына жауап береді. Жануарларға жүргізілген зерттеулерде пайдалы иммундық жауап пайда болып, компанияның «Matrix-M» көмегімен оннан жүз есеге дейін күшейтілгені анықталды иммунологиялық адъювант. Адамға жат приматтың вакцинаға реакциясын зерттеу басталды. 2015 жылдың ақпан айындағы жағдай бойынша[жаңарту], Новавакс бабундар мен макакаларға арналған екі приматты зерттеуді аяқтады және Австралияда I кезеңнің клиникалық сынақтарын бастады. Липидтік нанобөлшек (LNP) -капсулирленген сиРНҚ EBOV-тің Makona эпидемиялық штамын бағыттауға тез бейімделген және 100% қорғауға қабілетті резус маймылдары Жануарлар виремиялық және клиникалық ауру кезінде экспозициядан кейінгі үш күнде емдеу басталған кезде летальді қиындыққа қарсы.[59]І кезеңдегі адам сынақтарының нәтижелері көрсеткендей, адъюванцияланған Эбола GP вакцинасы барлық дозалар деңгейінде жоғары иммуногенді болды.[медициналық дәйексөз қажет ]
Мұрынға қарсы вакцина
2014 жылдың 5 қарашасында Хьюстон шежіресі жанындағы зерттеу тобы туралы хабарлады Техас-Остин университеті команда жеті жыл бойы жасаған эбола мұрынға арналған вакцина жасайтын болды.[60] Команда 2014 жылы жасаған приматтардың адамгершілікке жатпайтын зерттеулерінде вакцинаның инъекцияға қарағанда мұрынға арналған спрей арқылы тиімдірек болғанын хабарлады.[61] 2014 жылғы қарашадағы жағдай бойынша[жаңарту], қаржыландырудың жетіспеушілігінен команданың одан әрі дамуы екіталай болды.[60][62]
Ad5-EBOV
2014 жылдың аяғында және 2015 жылдың басында екі соқыр, рандомизацияланған I кезең сынақ өткізілді Цзянсу провинциясы Қытай; сот құрамында вакцинаны тексерді гликопротеидтер 1976 жылғы емес, 2014 жылғы штамм. Сынақ тиімділік сигналдарын тапты және қауіпсіздікке қатысты маңызды мәселелер туындамады.[45]
2017 жылы Қытай азық-түлік және дәрі-дәрмек басқармасы (CFDA) Биотехнология институтымен бірлесіп жасалған Эболаға қарсы вакцинаны мақұлдағанын жариялады Әскери медициналық ғылымдар академиясы және жеке вакцина жасаушы CanSino Biologics.[63] Оның құрамында адам бар аденовирус ЗЕБОВ-тан алынған гликопротеин генімен серотип 5 векторы (Ad5).[64] Олардың нәтижелері Африкада және Еуропада өткен rVSV-ZEBOV сынақтарымен сәйкес келді.[65]
Vaxart планшеті
Ваксарт Inc вакцина технологиясын температураға тұрақты таблетка түрінде жасайды, ол төмендеу сияқты артықшылықтар ұсына алады суық тізбек талап, және жылдам және масштабталатын өндіріс. 2015 жылдың қаңтарында Vaxart компаниясы Эболаға қарсы вакцинаны I кезеңге дейін әзірлеуге қаражат бөлгенін мәлімдеді.[66]
Эбола вирусын әлсірететін вакцина
Жылы жарияланған зерттеу Ғылым 2015 жылдың наурызында Эбола вирусының әлсіреген түрімен вакцинация адамнан тыс приматтарға белгілі бір қорғаныс беретінін көрсетті. Бұл зерттеу Ұлттық денсаулық сақтау институттарының жануарларды күту және пайдалану жөніндегі институционалды комитетімен бекітілген хаттамаға сәйкес жүргізілді.[67] Жаңа вакцина EBOVΔVP30 деп аталатын Эбола штаммына негізделген, ол оны қайталай алмайды.[50]
GamEvac-Combi
Жылы жарияланған зерттеу Адамға арналған вакциналар және иммунотерапевтика 2017 жылы наурызда Ресейдегі GamEvac-Combi вакцинасының клиникалық зерттеулерінің деректерін талдай отырып, вакцинаның қауіпсіз және тиімді екендігі туралы қорытынды шығарды және III кезең сынақтарына көшуді ұсынды.[68]
Перспективалар
2019 жылдың қыркүйек айында зерттеу жарияланды Ұяшық туралы есептер Эбола вирусы VP35 ақуызының оның иммунды жалтаруындағы рөлін көрсетті. Мутантты VP35 ақуызымен (VP35m) Эбола вирусының рекомбинантты түрі дамыды және RIG-I тәрізді рецепторлық сигнализацияны белсендіруде оң нәтиже көрсетті. Адам емес приматтарға VP35 әр түрлі дозалары қарсы болды. Бұл қиындық туа біткен иммундық жүйені белсендіруге және анти-ЭВОВ антиденелерін өндіруге әкелді. Содан кейін приматтар жабайы Эбола вирусына қарсы тұрды және тірі қалды. Бұл болашақ вакцинаны дамыту перспективасын тудырады.[69]
Батыс Африкадағы клиникалық сынақтар
2015 жылдың қаңтарында, Мари-Паул Киени, Дүниежүзілік денсаулық сақтау ұйымы Денсаулық сақтау жүйелері және инновациялар бойынша бас директордың көмекшісі (ДДҰ) cAd3-EBO Z және VSV-EBOV вакциналары ерте тестілеу кезінде қолайлы қауіпсіздік профилдерін көрсетті және жақын арада Либерия, Сьерра-Леоне, ауқымды сынақтарға жетеді деп мәлімдеді. және Гвинея. Сынақтарға 27000 адам қатысады және үш топтан тұрады - алғашқы екі топтың мүшелері екі үміткерден вакцина алады, ал үшінші топ - плацебо.[70] Екі вакцина содан бері сәтті аяқталды 2 кезең зерттеу. Ауқымды 3 кезең зерттеулер 2015 жылдың сәуір айынан басталды[жаңарту], Либерия мен Сьерра-Леонеде,[19][57] және Гвинеяда 2016 жылдың наурызында.[22]
Сонымен қатар, медициналық антрополог Монреаль университеті, Гвинеяда жұмыс істеген және сәуір айында Эболаны емдеу бөлімшелерінің бірінде уақыт өткізгеннен кейін сот процесінде қауіпсіздік туралы қосымша сұрақтар қойды, егер олар науқастар ауырып қалса, сотқа қатысушылар Кояядағы орталық, шамамен 50 Конакри астанасынан км.[17]
The Ресей Сыртқы істер министрлігі 2016 жылы 2000 адам қатысқан екі ресейлік вакцинаның далалық сынақтарын өткізу ниеті туралы хабарлады.[71] Жергілікті бұқаралық ақпарат құралдарының хабарлауынша, Гвинея үкіметі сот процестерін 2017 жылдың 9 тамызында бастауға рұқсат берген Русал - эпидемиология және микробиология ғылыми-диагностикалық орталығы Киндиа. Сынақтар 2018 жылға дейін жалғасады деп жоспарланған.[71][72] 2019 жылдың қазан айынан бастап Ресей вакцинаны жергілікті бақылаушы органдармен лицензиялады және вакцинаны Африкаға жіберуге дайын болды.[73]
АҚШ-тың ұлттық қоры
2014 жылы, Credit Suisse АҚШ үкіметі 1 доллардан астам қаражат береді деп есептеді Эбола вирусына қарсы дәрі-дәрмектер мен вакциналар жасау жөніндегі компанияларға жасалған келісімшарттар бойынша миллиард.[74] Конгресс 2004 жылы аурудың мүмкін ошақтары үшін вакциналар мен дәрі-дәрмектердің ұлттық қорын қаржыландыратын заң қабылдады.[74] Эбола вакциналарын бірқатар компаниялар жасайды деп күтілген: GlaxoSmithKline, NewLink генетикасы, Джонсон және Джонсон және Бавариялық скандинавия.[74] Басқа компания, Туындайтын БиоШешімдер, жаңа дозаларын шығаруға қатысушы болды ZMapp,[дәйексөз қажет ] бастапқыда Эбола вирусын емдеуге арналған дәрі Биофармацевтикалық карта.[75] ZMapp жеткізілімдері 2014 жылдың тамызында таусылды.[76] 2014 жылдың қыркүйегінде Биомедициналық жетілдірілген зерттеу және әзірлеу басқармасы (BARDA) ZMapp дамуын жеделдету үшін Mapp Biopharmaceutical компаниясымен миллиондаған долларлық келісімшарт жасады.[77] Қосымша келісімшарттар 2017 жылы жасалды.[78]
Сондай-ақ қараңыз
Әдебиеттер тізімі
- ^ а б c г. e f ж сағ мен j к л «Эбола вирусының алдын-алу үшін FDA мақұлдаған алғашқы вакцина, бұл халықтың денсаулығына дайындық пен жауап қайтарудың маңызды кезеңі». АҚШ Азық-түлік және дәрі-дәрмектерді басқару (FDA). 19 желтоқсан 2019. Мұрағатталды түпнұсқадан 2019 жылғы 20 желтоқсанда. Алынған 19 желтоқсан 2019.
 Бұл мақалада осы қайнар көздегі мәтін енгізілген қоғамдық домен.
Бұл мақалада осы қайнар көздегі мәтін енгізілген қоғамдық домен. - ^ McKee S (23 желтоқсан 2019). «АҚШ Merck's Эбола вакцинасын мақұлдады». PharmaTimes Online. Суррей, Англия: PharmaTimes Media Limited. Алынған 24 желтоқсан 2019.
- ^ Бет Мол (16 сәуір 2019). «Эбола эпидемиясы өршіп тұрған кезде вакцина 97,5% тиімді, 90-нан астам адамды қорғайды». Ars Technica.
- ^ Hoenen T, Groseth A, Feldmann H (шілде 2012). «Эболаға қарсы қазіргі вакциналар». Биологиялық терапия туралы сарапшылардың пікірі. 12 (7): 859–72. дои:10.1517/14712598.2012.685152. PMC 3422127. PMID 22559078.
- ^ Петерсон А.Т., Бауэр Дж.Т., Миллс Дж.Н. (қаңтар 2004). «Филовирус ауруының экологиялық-географиялық таралуы». Пайда болып жатқан инфекциялық аурулар. 10 (1): 40–47. дои:10.3201 / eid1001.030125. PMC 3322747. PMID 15078595.
- ^ Fausther-Bovendo H, Mulangu S, Sallivan NJ (маусым 2012). «Адамдар мен маймылдарға арналған эболавирустық вакциналар». Вирологиядағы қазіргі пікір. 2 (3): 324–29. дои:10.1016 / j.coviro.2012.04.003. PMC 3397659. PMID 22560007.
- ^ а б Павот V (желтоқсан 2016). «Эбола вирусына қарсы вакциналар: біз қайда тұрамыз?». Клиникалық иммунология. 173: 44–49. дои:10.1016 / j.clim.2016.10.016. PMID 27910805.
- ^ Marzi A, Hanley PW, Haddock E, Martellaro C, Kobinger G, Feldmann H (қазан 2016). «Весикулярлық стоматит вирусы-эбола вирусы, Макона эбола вирусымен жұқтырылған резус-макакаларда экспозициядан кейінгі емдеудің тиімділігі» (PDF). Инфекциялық аурулар журналы. 214 (3-қосымша): S360-66. дои:10.1093 / infdis / jiw218. PMC 5050468. PMID 27496978.
- ^ Марзи А, Робертсон С.Ж., Хэддок Е, Фельдманн Ф, Ханли П.В., Скотт Д.П. және т.б. (Тамыз 2015). «Эбола вакцинасы. VSV-EBOV макакаларды 2014/15 Эбола вирусының таралу штаммымен инфекциядан тез қорғайды». Ғылым. 349 (6249): 739–42. дои:10.1126 / science.aab3920. PMID 26249231.
- ^ «Merck's Ervebo [Эбола Заир вакцинасы (rVSVΔG-ZEBOV-GP) тікелей эфирде] Еуропалық Одақта шартты түрде мақұлданды» (Баспасөз хабарламасы). Мерк. 11 қараша 2019. Мұрағатталды түпнұсқадан 11 қараша 2019 ж. Алынған 11 қараша 2019 - Business Wire арқылы.
- ^ а б «ДДҰ эболаға қарсы вакцинаны алдын-ала біліктіліктен өткізіп, оны қауіпті елдерде қолдануға жол ашады» (Баспасөз хабарламасы). Дүниежүзілік денсаулық сақтау ұйымы. 12 қараша 2019. Мұрағатталды түпнұсқадан 2019 жылғы 15 қарашада. Алынған 13 қараша 2019.
- ^ а б c «Ervebo EPAR». Еуропалық дәрі-дәрмек агенттігі (EMA). 12 желтоқсан 2019. Алынған 1 шілде 2020. Мәтін © Еуропалық дәрі-дәрмек агенттігі болып табылатын осы дереккөзден көшірілді. Көшіру көзі танылған жағдайда рұқсат етіледі.
- ^ «Эрвебо». АҚШ Азық-түлік және дәрі-дәрмектерді басқару (FDA). 19 желтоқсан 2019. Алынған 1 шілде 2020.
- ^ «Эболаға қарсы канадалық вакцинаны әзірлеуді Мерк қабылдады». CBC жаңалықтары. 24 қараша 2014 ж. Алынған 25 қараша 2014.
- ^ Henao-Restrepo AM, Longini IM, Egger M, Dean NE, Edmunds WJ, Camacho A және т.б. (Тамыз 2015). «Эбола бетіндегі гликопротеинді білдіретін rVSV-векторлы вакцинаның тиімділігі мен тиімділігі: Гвинеяға сақина вакцинациясының кластерлік-рандомизацияланған сынамасының аралық нәтижелері». Лансет. 386 (9996): 857–66. дои:10.1016 / s0140-6736 (15) 61117-5. hdl:10144/575218. PMID 26248676. S2CID 40830730.
- ^ «Эбола вирусына қарсы вакцинаның бірнеше сынағы халықаралық ынтымақтастықпен жеделдетілді» (Баспасөз хабарламасы). Жақсы сенім. Алынған 29 қазан 2014.
- ^ а б Шучман М (мамыр 2015). «Африканың батысындағы эболаға қарсы вакцина сынақтары сынға ұшырайды». Лансет. 385 (9981): 1933–34. дои:10.1016 / s0140-6736 (15) 60938-2. PMID 25979835. S2CID 40400570.
- ^ Чан М. «ДДҰ бас директоры эболаға қарсы вакциналар бойынша жоғары деңгейлі кездесу ашады». Дүниежүзілік денсаулық сақтау ұйымы (ДДСҰ). Алынған 10 қаңтар 2015.
- ^ а б c «Эбола вирусына қарсы вакциналар Либерияның 2-ші кезеңінде қауіпсіз болып көрінеді» (Баспасөз хабарламасы). Ұлттық денсаулық сақтау институттары (NIH). 26 наурыз 2015 ж.
- ^ Henao-Restrepo AM, Longini IM, Egger M, Dean NE, Edmunds WJ, Camacho A және т.б. (Тамыз 2015). «Эбола бетіндегі гликопротеинді білдіретін rVSV-векторлы вакцинаның тиімділігі мен тиімділігі: Гвинеяға сақина вакцинациясының кластерлік-рандомизацияланған сынақ нәтижелері». Лансет. 386 (9996): 857–66. дои:10.1016 / S0140-6736 (15) 61117-5. hdl:10144/575218. PMID 26248676. S2CID 40830730.
- ^ «Эбола жаңартуы (93): вакцинаның сынақ нәтижелері оң». ProMED поштасы. Халықаралық жұқпалы аурулар қоғамы. Алынған 2 тамыз 2015.
- ^ а б «Дүниежүзілік денсаулық сақтау ұйымы Гвинеядағы эбола өршуін болдырмау үшін контактілерге вакцинациялауды үйлестіреді». Дүниежүзілік денсаулық сақтау ұйымы (ДДСҰ). Наурыз 2016. Алынған 14 мамыр 2016.
- ^ «Әлем эболаға қарсы вакцинаның қарсаңында» (Баспасөз хабарламасы). Дүниежүзілік денсаулық сақтау ұйымы (ДДСҰ). 31 шілде 2015.
- ^ а б Henao-Restrepo AM, Camacho A, Longini IM, Watson CH, Edmunds WJ, Egger M және т.б. (Ақпан 2017). «Эбола вирусының алдын алудағы rVSV-векторлы вакцинаның тиімділігі мен тиімділігі: Гвинеяға сақина вакцинациясының қорытынды нәтижелері, ашық этикеткалар, кластерлік рандомизацияланған сынақ (Ebola Ça Suffit!)». Лансет. 389 (10068): 505–18. дои:10.1016 / S0140-6736 (16) 32621-6. PMC 5364328. PMID 28017403.
- ^ а б Berlinger J (22 желтоқсан 2016). «Эболаға қарсы вакцина 100% қорғайды, зерттеу нәтижелері бойынша». CNN. Алынған 27 желтоқсан 2016.
- ^ а б «Сынақтың қорытынды нәтижелері Эболаға қарсы вакцинаның аурудан жоғары қорғаныс беретіндігін растайды» (Баспасөз хабарламасы). Дүниежүзілік денсаулық сақтау ұйымы. 23 желтоқсан 2016. Мұрағатталды түпнұсқадан 11 қараша 2019 ж. Алынған 11 қараша 2019.
- ^ Metzger WG, Vivas-Martínez S (наурыз 2018). «RVSV-ZEBOV эбола вакцинасының күмәнді тиімділігі». Лансет. 391 (10125): 1021. дои:10.1016 / S0140-6736 (18) 30560-9. PMID 29565013.
- ^ а б «Merck's Ervebo [Эбола Заир вакцинасы (rVSVΔG-ZEBOV-GP) тікелей эфирде] Еуропалық Одақта шартты түрде мақұлданды» (Баспасөз хабарламасы). Мерк. 11 қараша 2019. Мұрағатталды түпнұсқадан 11 қараша 2019 ж. Алынған 11 қараша 2019 - Business Wire арқылы.
- ^ а б «Zabdeno EPAR». Еуропалық дәрі-дәрмек агенттігі (EMA). 26 мамыр 2020. Алынған 23 шілде 2020.
- ^ а б «Mvabea EPAR». Еуропалық дәрі-дәрмек агенттігі (EMA). 26 мамыр 2020. Алынған 23 шілде 2020.
- ^ «Джонсон мен Джонсон Еуропалық комиссияның Янсенге қарсы эбола профилактикалық вакцинасын мақұлдауын жариялайды» (Баспасөз хабарламасы). Джонсон және Джонсон. 1 шілде 2020. Алынған 16 шілде 2020 - Reuters арқылы.
- ^ а б Бавариялық скандинавия (15 шілде 2015). «Бавария Nordic Оксфорд вакциналар тобы MVA-BN Filo және Janssen's Advac технологияларын біріктіретін Эболаға қарсы вакцина режимін 2-кезеңінде зерттеуді бастағанын хабарлайды» (Баспасөз хабарламасы). Копенгаген, Дания: Бавариялық Скандинавия. Алынған 16 шілде 2015.
- ^ а б Клиникалық зерттеу нөмірі NCT02313077 «Дені сау қатысушылардағы гетерологиялық Премьер-Boost Эбола вакцина режимін қауіпсіздігі мен иммуногендігін зерттеу» үшін ClinicalTrials.gov
- ^ Уолш Ф (6 қаңтар 2015). «Эбола: вакциналарға арналған жаңа сынақ басталды». BBC News Online. Алынған 6 қаңтар 2015.
- ^ «Джонсон мен Джонсон эболаға қарсы вакцинаны жеделдету және өндірісті айтарлықтай кеңейту бойынша негізгі міндеттемелерін жариялады» (Баспасөз хабарламасы). Джонсон және Джонсон. Алынған 6 қаңтар 2015.
- ^ Hirschler B (9 қазан 2015). «J&J вакцина сынақтарын Сьерра-Леонеде бастайды, тіпті Эбола азайған кезде де». Reuters. Алынған 15 қазан 2015.
- ^ а б «Джонсон мен Джонсон Янсанның тергеу эболасына қарсы вакцина режиміне Еуропалық маркетингтік авторизациялау өтінімдерін жіберетіндігін хабарлайды». Янсен. 17 қараша 2019. Мұрағатталды түпнұсқадан 2019 жылғы 17 қарашада. Алынған 16 қараша 2019.
- ^ Harper R (12 қараша 2019). «Эболаға қарсы вакцина режиміне ЕО-ның маркетингтік авторизациясы ұсынылды». Еуропалық фармацевтикалық шолу. Мұрағатталды түпнұсқадан 2019 жылғы 17 қарашада. Алынған 16 қараша 2019.
- ^ а б c г. «Эбола вирусының алдын алу үшін жаңа вакцина Еуропалық Одақта мақұлдануға ұсынылады». Еуропалық дәрі-дәрмек агенттігі (EMA) (Баспасөз хабарламасы). 29 мамыр 2020. Алынған 29 мамыр 2020. Мәтін © Еуропалық дәрі-дәрмек агенттігі болып табылатын осы дереккөзден көшірілді. Көшіру көзі танылған жағдайда рұқсат етіледі.
- ^ «Zabdeno: EC шешімі күтілуде». Еуропалық дәрі-дәрмек агенттігі (EMA). 29 мамыр 2020. Алынған 29 мамыр 2020. Мәтін © Еуропалық дәрі-дәрмек агенттігі болып табылатын осы дереккөзден көшірілді. Көшіру көзі танылған жағдайда рұқсат етіледі.
- ^ «Mvabea: EC шешімі күтілуде». Еуропалық дәрі-дәрмек агенттігі (EMA). 29 мамыр 2020. Алынған 29 мамыр 2020. Мәтін © Еуропалық дәрі-дәрмек агенттігі болып табылатын осы дереккөзден көшірілді. Көшіру көзі танылған жағдайда рұқсат етіледі.
- ^ ЧАРСКА-ТОРЛИ, Дагмара (29 мамыр 2020). «Эбола вирусының алдын алу үшін жаңа вакцина Еуропалық Одақта мақұлдануға ұсынылады». Еуропалық дәрі-дәрмек агенттігі (EMA). Алынған 7 шілде 2020.
- ^ «Дүниежүзілік денсаулық сақтау ұйымы Гвинеядағы эбола өршуін болдырмау үшін контактілерге вакцинациялауды үйлестіреді». Дүниежүзілік денсаулық сақтау ұйымы (ДДСҰ). Алынған 20 шілде 2016.
- ^ «Вакциналар альянсы Merck-тің Эбола ауруымен ауырғаны үшін 5 миллион доллар алдын-ала келісімге қол қойды». Reuters. 20 қаңтар 2016 ж. Алынған 20 шілде 2016.
- ^ а б Zhu FC, Hou LH, Li JX, Wu SP, Liu P, Zhang GR, және басқалар. (Маусым 2015). «Қытайдағы сау ересектердегі жаңа рекомбинантты аденовирустық типтегі 5-векторлы Эбола вакцинасының қауіпсіздігі және иммуногендігі: рандомизацияланған, екі соқыр, плацебо-бақыланатын, 1 фазалық сынақтың алдын-ала есебі». Лансет. 385 (9984): 2272–79. дои:10.1016 / S0140-6736 (15) 60553-0. PMID 25817373. S2CID 34636122.
- ^ Миллиган ID, Gibani MM, Sewell R, Clutterbuck EA, Campbell D, Plested E және т.б. (Сәуір 2016). «Аденовирустық 26 типті және модификацияланған вакцинаның Анкара-Векторлық Эбола вакциналарының қауіпсіздігі және иммуногендігі: кездейсоқ клиникалық сынақ». Джама. 315 (15): 1610–23. дои:10.1001 / jama.2016.4218 ж. PMID 27092831.
- ^ «Эболаға қарсы вакциналар, терапия және диагностика». Дүниежүзілік денсаулық сақтау ұйымы (ДДСҰ). 6 шілде 2015. Алынған 10 қыркүйек 2015.
- ^ Блейни Дж.Е., Марзи А, Уиллет М, Папанери А.Б., Вирблих С, Фельдманн Ф және т.б. (30 мамыр 2015). «Құтыру вирусына негізделген екі валентті вакцинамен иммунизацияланған адамнан тыс приматтардағы антиденелердің сапасы және өлімге әкелетін Эбола вирусынан қорғаныс». PLOS қоздырғыштары. 9 (5): e1003389. дои:10.1371 / journal.ppat.1003389. PMC 3667758. PMID 23737747.
- ^ «КТ зертханасы эболаның таралуын тоқтатады деп үміттенеді». 3 наурыз 2015. Алынған 10 қыркүйек 2015.
- ^ а б Marzi A, Halfmann P, Hill-Batorski L, Feldmann F, Shupert WL, Neumann G, et al. (Сәуір 2015). «Вакциналар. Эбола вирусына қарсы вакцина адамгершілікке жатпайтын приматтарда қорғайды». Ғылым. 348 (6233): 439–42. дои:10.1126 / science.aaa4919. PMC 4565490. PMID 25814063.
- ^ Вакциналарды зерттеу орталығы, NIAID (2 қазан 2014). «Эбола вакцинасының клиникалық дамуына шолу (презентация)» (PDF). Дүниежүзілік денсаулық сақтау ұйымы (ДДСҰ). Алынған 21 қазан 2014.
- ^ Клиникалық зерттеу нөмірі NCT02344407 «Либериядағы эбола вакциналарын зерттеу жөніндегі серіктестік (PREVAIL)» үшін ClinicalTrials.gov
- ^ Ledgerwood JE, DeZure AD, Stanley DA, Coates EE, Novik L, Enama ME және т.б. (Наурыз 2017). «Аденовирусты вирустық эбола вирусына қарсы вакцина». Жаңа Англия медицинасы журналы. 376 (10): 928–38. дои:10.1056 / NEJMoa1410863. PMID 25426834.
- ^ Стэнли Д.А., Хонко А.Н., Асиеду С, Трефри Дж.К., Лау-Килби А.В., Джонсон Дж.К. және т.б. (Қазан 2014). «Шимпанзе аденовирусына қарсы вакцина эболавирусқа қарсы жедел және берік қорғаныс иммунитетін тудырады». Табиғат медицинасы. 20 (10): 1126–29. дои:10.1038 / нм.3702. PMID 25194571. S2CID 20712490.
- ^ Клиникалық зерттеу нөмірі NCT02240875 «Жаңа эбола вакциналарын бағалауға арналған зерттеу, cAd3-EBO Z және MVA-BN Filo» үшін ClinicalTrials.gov
- ^ Оксфорд университеті (4 желтоқсан 2014). «Эбола вирусына қарсы вакцина Оксфорд университетінде алғашқы сынақтарға кірісті». Алынған 7 желтоқсан 2014.
- ^ а б «Эболаға қарсы вакцинаны сынақтан өткізу Сьерра-Леонда басталды» (Баспасөз хабарламасы). Ауруларды бақылау және алдын алу орталықтары (CDC). 14 сәуір 2015 ж.
- ^ Gire SK, Goba A, Андерсен KG, Sealfon RS, Park DJ, Kanneh L және т.б. (Қыркүйек 2014). «Геномдық қадағалау 2014 жылғы эпидемия кезінде Эбола вирусының шығу тегі мен таралуын анықтайды». Ғылым. 345 (6202): 1369–72. Бибкод:2014Sci ... 345.1369G. дои:10.1126 / ғылым.1259657. PMC 4431643. PMID 25214632.
- ^ Thi EP, Mire CE, Lee AC, Geisbert JB, Zhou JZ, Agans KN және т.б. (Мамыр 2015). «Эбола вирусын-Макона жұқтырған адамнан тыс приматтарды липидті нанобөлшек siRNA емдеу». Табиғат. 521 (7552): 362–65. Бибкод:2015 ж. 521..362T. дои:10.1038 / табиғат 14442. PMC 4467030. PMID 25901685.
- ^ а б Ackerman T (5 қараша 2014). «Эболаға қарсы мұрынға арналған спрей вакцинасы маймылдарда тиімді». Хьюстон шежіресі. Алынған 13 қараша 2014.
- ^ Choi JH, Jonsson-Schmunk K, Qiu X, Shedlock DJ, Strong J, Xu JX және т.б. (Тамыз 2015). «Аденовирусқа негізделген бір реттік тыныс алу рекомбинантты вакцина адамнан тыс приматтарды летальды эбола инфекциясынан қорғауды қамтамасыз етеді». Молекулалық фармацевтика. 12 (8): 2712–31. дои:10.1021 / mp500646d. PMC 4525323. PMID 25363619.
- ^ Stanton D (12 қараша 2014). «Эбола мұрынына қарсы вакцина қаржыландыру құрғап кету қаупі бар». PharmaTechnologist. Кроули, Сассекс, Ұлыбритания: Уильям Рид Бизнес Медиа. Алынған 13 қараша 2014.
- ^ Фэн С (20 қазан 2017). «Қытай эболаға қарсы вакцинаны мақұлдады». Caixin Global. Архивтелген түпнұсқа 7 қазан 2018 ж. Алынған 7 қазан 2018.
- ^ Вонг Г, Мендоза Э.Дж., Пламмер Ф.А., Гао Г.Ф., Кобингер Г.П., Циу Х (ақпан 2018). «Орындықтан дерлік төсекке дейін: лицензияланған Эбола вирусына қарсы вакцинаға дейінгі жол». Биологиялық терапия туралы сарапшылардың пікірі. 18 (2): 159–73. дои:10.1080/14712598.2018.1404572. PMC 5841470. PMID 29148858.
- ^ Hackett DW (31 наурыз 2018). «АҚШ пен Қытай арасында» Эбола «вакцинасын дамыту бойынша жарыс». Дәлдікпен вакцинациялау.
- ^ «Vaxart даму портфолиосын қаржыландыру үшін қаржыландыруды аяқтайды». Ваксарт. Архивтелген түпнұсқа 2015 жылғы 19 қаңтарда. Алынған 19 қаңтар 2015.
- ^ Marzi A, Feldmann F, Geisbert TW, Feldmann H, Safronetz D (ақпан 2015). «Ласса және Эбола вирустарына қарсы везикулярлық стоматит вирусына негізделген вакциналар». Пайда болып жатқан инфекциялық аурулар. 21 (2): 305–07. дои:10.3201 / eid2102.141649. PMC 4313664. PMID 25625358.
- ^ Должикова И.В., Зубкова О.В., Тухватулин А.И., Джаруллаева А.С., Тухватулина Н.М., cheебляков Д.В. және т.б. (Наурыз 2017). «GamEvac-Combi, гетерологиялық VSV және Ad5-векторлы эбола вакцинасының қауіпсіздігі және иммуногендігі: Ресейдегі сау ересектердегі I / II ашық фазасы». Адамға арналған вакциналар және иммунотерапевтика. 13 (3): 613–20. дои:10.1080/21645515.2016.1238535. PMC 5360131. PMID 28152326.
- ^ Woolsey C, Menicucci AR, Cross RW, Luthra P, Agans KN, Borisevich V және т.б. (Қыркүйек 2019). «VP35 мутантты эбола вирусына вируленттілік жетіспейді, бірақ вирустың жабайы түріне қарсы қорғаныс иммунитеті болуы мүмкін». Ұяшық туралы есептер. 28 (12): 3032-46.e6. дои:10.1016 / j.celrep.2019.08.047. PMC 6886687. PMID 31533029.
- ^ «Ұлыбритания эболаға қарсы вакцина сынақтарын жүргізеді. Ars Technica. Алынған 10 қаңтар 2015.
- ^ а б «Ресей Эболаға қарсы вакцина сынақтарын қаржыландырады». Алынған 14 қыркүйек 2017.
- ^ «Гвинея: Эбола вирусына қарсы вакциналар және вирустың пайда болуы - Африка 7-серия: Африка және Африкада». www.afrique-sur7.fr (француз тілінде). Алынған 14 қыркүйек 2017.
- ^ «Ресей Африкаға Эбола вакцинасын жеткізуге дайын». ТАСС. Алынған 1 қараша 2019.
- ^ а б c Руни Б (28 қазан 2014). «Эбола: 1 миллиард долларлық дәрі жасау». CNN. Алынған 19 қараша 2014.
- ^ Gantz S (20 қазан 2014). «Эбола дәрі-дәрмектерін өндіруді қарастырудағы үшеуінің арасында туындайтын BioSolutions». Балтимор іскери журналы. Алынған 13 қараша 2014.
- ^ Бернштейн Л, Деннис Б (11 тамыз 2014). «Африкаға жеткізілгеннен кейін Эбола сынағына қарсы дәрі-дәрмекпен қамтамасыз ету» таусылды «дейді АҚШ компаниясы». Washington Post. Алынған 17 қараша 2019.
- ^ МакКарти М (қыркүйек 2014). «АҚШ Эбола препаратының дамуын жеделдету үшін ZMapp өндірушісімен келісімшартқа отырды». BMJ. 349 (sep04 10): g5488. дои:10.1136 / bmj.g5488. PMID 25189475.
- ^ «MappBio BARDA-мен ZMapp және қосымша филовирустық медициналық шараларға келісімшарттар жариялайды» (Баспасөз хабарламасы). Биофармацевтикалық карта. 29 қыркүйек 2017 ж. Мұрағатталды түпнұсқадан 2019 жылғы 17 қарашада. Алынған 16 қараша 2019.
Әрі қарай оқу
- Фарук Ф, Бек К, Паолино К.М., Филлипс Р, Уотерс НК, Регулярлар Дж.А., Бергманн-Лейтнер ES (маусым 2016). «RVSV-ZEBOV Эбола вакцинасымен вакцинациядан кейінгі адамдардағы циркуляциялық фолликулярлық Т-көмекші жасушалар және цитокин профилі». Ғылыми баяндамалар. 6: 27944. Бибкод:2016 жыл НАТСР ... 627944F. дои:10.1038 / srep27944. PMC 4914957. PMID 27323685.
- Салливан Н, Янг З.Я., Набель Г.Дж. (қыркүйек 2003). «Эбола вирусының патогенезі: вакциналар мен терапияның салдары». Вирусология журналы. 77 (18): 9733–7. дои:10.1128 / JVI.77.18.9733-9737.2003. PMC 224575. PMID 12941881.
- Diakite I, Mooring EQ, Velásquez GE, Мюррей МБ (тамыз 2016). «Кеңістіктік құрылымдалған математикалық модельді қолданып, эбола вакцинасының тиімділігін анықтауға арналған роман тәрізді сатылы кластердің сынақ жобалары». PLOS елемейтін тропикалық аурулар. 10 (8): e0004866. дои:10.1371 / journal.pntd.0004866. PMC 4979980. PMID 27509037.
- Cazares LH, Ward MD, Brueggemann EE, Kenny T, Demond P, Mahone CR және т.б. (5 қыркүйек 2016). «Эбола вирусына ұқсас бөлшектерге қарсы вакцина препараттарындағы вирустық қабықтағы гликопротеин мөлшерін анықтауға арналған сұйықтық хроматографиясы жоғары рұқсатты масс-спектрометрия әдісін әзірлеу». Клиникалық протеомика. 13 (1): 18. дои:10.1186 / s12014-016-9119-8. PMC 5011338. PMID 27597813.
- Konduru K, Shurtleff AC, Bradfute SB, Nakamura S, Bavari S, Kaplan G (13 қыркүйек 2016). «Ebolavirus Glycoprotein Fc протеині Гвинея шошқаларын өлімге шақырудан қорғайды». PLOS ONE. 11 (9): e0162446. Бибкод:2016PLoSO..1162446K. дои:10.1371 / journal.pone.0162446. PMC 5021345. PMID 27622456.
- Cheng F, Murray JL, Zhao J, Sheng J, Zhao Z, Rubin DH (қыркүйек 2016). «Ген-тұзақ инерциональды мутагенезімен анықталған жасушалық вирусқа қарсы дәрі-дәрмектерді жүйелік биологияға негізделген зерттеу». PLOS есептеу биологиясы. 12 (9): e1005074. Бибкод:2016PLSCB..12E5074C. дои:10.1371 / journal.pcbi.1005074. PMC 5025164. PMID 27632082.
- Olowookere SA, Abioye-Kuteyi EA, Adekanle O (қараша 2016). «Эбола вирусына қарсы вакцина сынақтарына қатысуға және Нигерияның оңтүстік-батысында Иле-Ифедегі үшінші ауруханада медициналық қызметкерлердің вакцинациясын қабылдауға дайын болу». Вакцина. 34 (47): 5758–5761. дои:10.1016 / j.vaccine.2016.10.004. PMID 27751640.
- Павот V (желтоқсан 2016). «Эбола вирусына қарсы вакциналар: біз қайда тұрамыз?». Клиникалық иммунология. 173: 44–49. дои:10.1016 / j.clim.2016.10.016. PMID 27910805.
- Wellcome Trust - CIDRAP Эбола вакцина тобы B (қаңтар 2017). Эбола вакциналарын жасауды аяқтау: қазіргі жағдайы, қалған мәселелер және ұсыныстар. Инфекциялық ауруларды зерттеу және саясат орталығы (CIDRAP) және Wellcome Trust. Мұрағатталды (PDF) түпнұсқадан 2017 жылғы 18 қаңтарда. Алынған 18 қаңтар 2017.
- Розалес-Мендоза С, Нието-Гомес Р, Ангуло С (1 қаңтар 2017). «Эбола вирусына қарсы күресте өсімдік вакциналарын дамыту перспективасы». Иммунологиядағы шекаралар. 8: 252. дои:10.3389 / fimmu.2017.00252. PMC 5344899. PMID 28344580.
Сыртқы сілтемелер
- Эболаға қарсы вакциналар АҚШ ұлттық медицина кітапханасында Медициналық тақырып айдарлары (MeSH)
| Шолия бар Тақырып үшін профиль Эболаға қарсы вакцина. |
