Каптодативті әсер - Captodative effect

The капдодативті әсер болып табылады тұрақтандыру туралы радикалдар синергетикалық әсерімен электронды алу орынбасар және электронды донорлық алмастырғыш.[2][3] Бұл атау электрондарды бөліп алатын топты (EWG) кейде «каптор» тобы деп атайды, ал электронды донорлық топ (EDG) «дативті» орынбасар болып табылады.[3] Олефиндер осы алмастырғыш үлгісімен бір кездері кастодативті деп сипатталады.[2] Радикалды реакциялар бірнеше химиялық реакцияларда ажырамас рөл атқарады және олар үшін де маңызды полимер туралы ғылым.[4]
EDG және EWG радикалды орталықтың жанында болған кезде радикалды орталықтың тұрақтылығы артады.[1] Орынбасарлар жасай алады кинетикалық алдын-алу арқылы радикалды орталықтарды тұрақтандыру молекулалар және басқа радикалды орталықтардың орталықпен әрекеттесуінен.[3] Орынбасарлар радикалды ионды делокализации арқылы центрді термодинамикалық тұрақтандырады резонанс.[1][3] Бұл тұрақтандыру механизмдері бос радикалды реакциялардың жылдамдығын арттырады.[5] Оң жақтағы суретте радикал кэптор арасында делокализацияланған нитрил (-CN), ал екінші дәрежелі амин (-N (CH3)2), осылайша радикалды орталықты тұрақтандырады.[3]
Реакция жылдамдығына орынбасушы әсер
Белгілі бір алмастырғыштар радикалды орталықтарды тұрақтандыруда басқаларға қарағанда жақсы.[6] Бұған орынбасардың ішіндегі радикалды ионды делокализациялау қабілеті әсер етеді өтпелі мемлекеттік құрылым.[3] Радикалды ионды делокализациялау өтпелі күй құрылымын тұрақтандырады. Нәтижесінде активтену энергиясы төмендейді, жалпы реакция жылдамдығы күшейеді. Каптодативті эффектке сәйкес, реакция жылдамдығы, егер EDG де, EWG де өтпелі күй құрылымында радикалды ионды делокализациялауға қабілетті болса.[7]
Ito және оның әріптестері артилтил радикалының бөлінген олефиндерге қосылу реакциясының жылдамдығын бақылаған.[6] Олефиндерде EWG болды нитрил топтық және әр түрлі ЭДГ және әр түрлі ЭДГ-дің қосылу реакцияларының жылдамдығына әсері байқалды. Зерттелген процесс:
Қосылу реакциясының жылдамдығы келесі ЭДГ-мен жоғарылайды: H
Синтезде қолданады
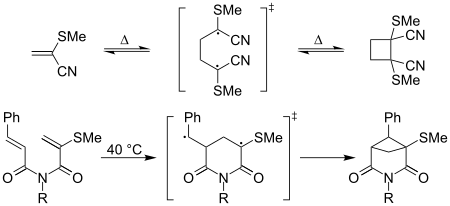
Контексінде «каптодативті этилендер» термині қолданылған циклдік шығарылым каптодативті радикалды аралықтардың қатысуымен жүретін реакциялар - мысалы, термиялық [2 + 2] бастан-аяқ димеризация 2-метилтиоакрилонитрил бөлме температурасында тез пайда болады; циклобитанның эквивалентті туындысының түзілуі акрилонитрил «жалқау».[8] Интрамолекулалық [2 + 2] циклизациялардың каптодативті эффектілермен күшейгені туралы да хабарланған,[8] төменде көрсетілгендей:
Ұқсас әсерлер [3 + 2], [4 + 2] және [3 + 4] сияқты басқа циклодредукциялар үшін де қарастырылды.[9] Сияқты жағдайлар туралы да хабарланған Дильс-Алдер және Фридель-қолөнер өтпелі күйге жатқызылған, нуклеофильді олефиндер тиімсіз реакция жасайтын реакциялар, бірадикальға жақын және осылайша тұрақталған.[8][10] Бұл зерттеулер Δω-ге, электрфильділіктің айырмашылығына және реакцияның полярлық сипатына тікелей тәуелділікті анықтады. Олар осы реакциялардың ішінде өте реактивті, стереоселективті, региоселективті болғандықтан қолданылды.[9][11]
Каптодативті олефиндер реакцияларда типтікке кедергі әсерін де көрсетеді изотоптық кинетикалық әсер, изотоппен белгіленген молекулалармен типтік емес реакциялардың пайда болуына мүмкіндік береді[12] және осы реакциялардың механизмдері мен өтпелі күйлері әсер еткендігін көрсету.
Полимерді қолдану
Еркін радикалды полимеризация, онда радикалдар процестің таралуындағы тізбекті тасымалдаушылар болып табылады, 2001 жылы АҚШ-та өндірілген 110 миллиард фунт полимерлердің 40 миллиардын құрады.[13] Каптодативті олефиндердің радикалды тұрақсыздандыратын әсер етпестен еріткіш әсеріне жауап беруінің ерекше артықшылығы бар.[4] Олар өздігінен радикалды өзгеріске ұшырайтындығын көрсетті, бұл полимерлеу механизмін түсіндіруде пайдалы болуға және жақсы түсінуге мүмкіндік береді. NMR зерттеулер. Сонымен қатар, каптодативті этандар молекулалық массаны үлестіру мен қалыптастыру блогын беретін ерекше қасиеттері бар бастамашылар болып табылады сополимерлер белгілі радикалды механизмдер арқылы. Каптодативті түрде алмастырылған бастапқы материалдардан алынған полимерлер оптикалық белсенділік, полярлықтағы айырмашылықтар сияқты «қалаулы» қасиеттерді көрсетеді. еріткіштің жақындығы, жылу және механикалық тұрақтылық.


- Полярлық алмастырғыштары бар полимерлердің қызықты қосымшалары бар, олардың ішінде электрлік және оптикалық материалдар.
- Бұл полимерлер әдетте мөлдір болады.
- Тди (бастапқы ыдырау) осы полимерлердің аналогтарымен салыстырғанда салыстырмалы түрде аз, бірақ T-ге қарағанда жоғарыдм (салмақтың өзгеру температурасының максималды жылдамдығы). Бұл дегеніміз, олар тезірек ери бастайды, бірақ фазаларды толығымен өзгертуге көп уақыт кетеді.
- Бастапқы материалдардың үлкен кадаптативті тұрақтандырғыштары бар полимерлер қыздыру кезінде бастапқы мономерге тез «айналады».
- Көпфункционалды әр мономер бірлігінде екі түрлі функционалды топтары бар полимерлер көбінесе каптодативті мономерлерден түзіледі.
- Туа біткен топтар ерігіштігін айтарлықтай өзгертеді Сутектік байланыс нақты екіфункционалды полимерлерде (жоғарыдағы суретті қараңыз). Алайда, қазіргі кезде нақты корреляция жасалынбаған, өйткені алмастырғыштар мен ерігіштіктердің барлық тіркесімдері зерттелмеген.
- Каптодативті полимер белгілі бір металдар бар хелаттарда жоғары функционалды.[4]
Әдебиеттер тізімі
- ^ а б c Анслин, Е.В .; Dougherty, D. A. (2006). Қазіргі физикалық органикалық химия (Додр. Ред.). Саусалито, Калифорния: Университеттің ғылыми кітаптары. ISBN 9781891389313.
- ^ а б Химияның қысқаша сөздігі. V&S баспалары. 2012. б. 51. ISBN 9789381588628.
- ^ а б c г. e f Вихе, Х. Г .; Яноусек, З .; Мерении, Р .; Стелла, Л. (1985). «Каптодативті әсер». Химиялық зерттеулердің есептері. 18 (5): 148–154. дои:10.1021 / ar00113a004.
- ^ а б c Танака, Х. (2003). «Полимер ғылымындағы каптодативті модификация». Полимер ғылымындағы прогресс. 28 (7): 1171–1203. дои:10.1016 / S0079-6700 (03) 00013-3.
- ^ Сустманн, Р .; Корт, Х.-Г. (1990). Физикалық органикалық химия жетістіктері. Сан-Диего, Калифорния: Academic Press. 131–172 бет. ISBN 0120335263.
- ^ а б c Ито, Осаму; Арито, Ю .; Мацуда, М. (1988). «Арилтихилдің радикалдың бөлінген олефиндерге қосылу жылдамдығына каптодативті әсері». Химиялық қоғам журналы, Perkin Transaction 2 (6): 869–873. дои:10.1039 / P29880000869.
- ^ Крери, Х .; Мехришейх-Мохаммади, М.Э. (1985). «Метиленециклопропанды қайта құру кезіндегі каптодативті жылдамдықты арттыру». Органикалық химия журналы. 51 (14): 2664–2668. дои:10.1021 / jo00364a009.
- ^ а б c Стелла, Л. (1986). «Циклодред реакцияларындағы каптодативті орынбасушы әсерлер». Вихеде Х.Г .; Яноусек, З .; Мерении, Р. (ред.) Радикалды химиядағы орынбасушы әсерлер. Спрингер. 361-370 бет. ISBN 9789027723406.
- ^ а б Эррера, Р .; Хименес-Васкес, Х. А .; Делгадо, Ф .; Содерберг, Б. Тамариз, Дж. (2005). «1-ацетивинил акрилаты: Дипель-Альдер мен Фридель-Қолөнер реакциясындағы электрон жетіспейтін қос облигацияға қатысты каптодативтің салыстырмалы реактивтілігін бағалауға арналған жаңа капотативті олефиндер және ішкі зонд». Бразилия химиялық қоғамының журналы. 16 (3A): 456-466. дои:10.1590 / S0103-50532005000300021.
- ^ Стелла, Л .; Баучер, Дж. (1982). «Капто-дативті орынбасушы әсерлер. 121 - Диелс-Алдер циклотредукцияларына арналған жаңа кетендік эквиваленттер ». Тетраэдр хаттары. 22 (9): 953–956. дои:10.1016 / S0040-4039 (00) 86992-0.
- ^ Доминго, Л .; Чаморро, Э .; Pérez, P. (2008). «Каптодативті этилендердің полярлық циклодредукция реакцияларындағы реактивтілігін түсіну. Теориялық зерттеу». Органикалық химия журналы. 73 (12): 4615–4624. дои:10.1021 / jo800572a. hdl:10533/139635. PMID 18484771.
- ^ Вуд, М .; Биссириу, С .; Лоу, С .; Windeatt, K. M. (2013). «Сутегі атомын беру кезінде біріншілік кинетикалық изотоптық эффект синтетикалық қолдану: Каптодативті тұрақтандырылған радикалдардың генерациясы». Органикалық және биомолекулалық химия. 11 (16): 2712–23. дои:10.1039 / C3OB40275D. PMID 23479029.
- ^ Одиан, Г. (2004). Полимерлеу принциптері (4-ші басылым). Нью-Йорк: Вили-Интерсиснис. ISBN 9780471274001.